Caroline Frädrich und Prof. Dr. Josef Köhrle von der Charité Berlin1 werden zusammen mit ihrem Forschungspartner Dr. Kostja Renko vom Bundesinstitut für Risikobewertung (BfR) für die Entwicklung einer Hochdurchsatz-Plattform zur Detektion von hormonwirksamen Substanzen geehrt2. Mit der neuen Plattform hat das Forscherteam 22.000 bekannte und unbekannte Substanzen, also Arzneimittel, pharmakologisch aktive Verbindungen, Umweltchemikalien und Molekülstrukturfragmente, auf ihren Einfluss auf die Schilddrüsenhormone untersucht. Dafür machten sie sich ein Verfahren aus der Redoxchemie zur photometrischen Iodbestimmung zunutze und entwickelten hieraus den Diodinase II-Hochdurchsatz-Assay (DIO2-HTS-Assay).
Drei Enzyme, die Deiodinasen 1-3 (DIO1-3), sind wesentliche Bestandteile des Schilddrüsen-hormonstoffwechsels3. Sie können Schilddrüsenhormone aktivieren oder inaktivieren, indem sie an unterschiedlichen Stellen Iodatome aus den Schilddrüsenhormonen entfernen. So überführen die Deiodinasen 1 und 2 durch Entfernen eines Iodatoms das wenig aktive Thyroxin (mit vier Iodatomen, T4) in ein aktives Triiodthyronin (mit drei Iodatomen, T3)4. Die Schilddrüsenhormone gelangen über das Blut zu den spezifischen Rezeptoren der Zellen und beeinflussen dort die Stoffwechselaktivität. 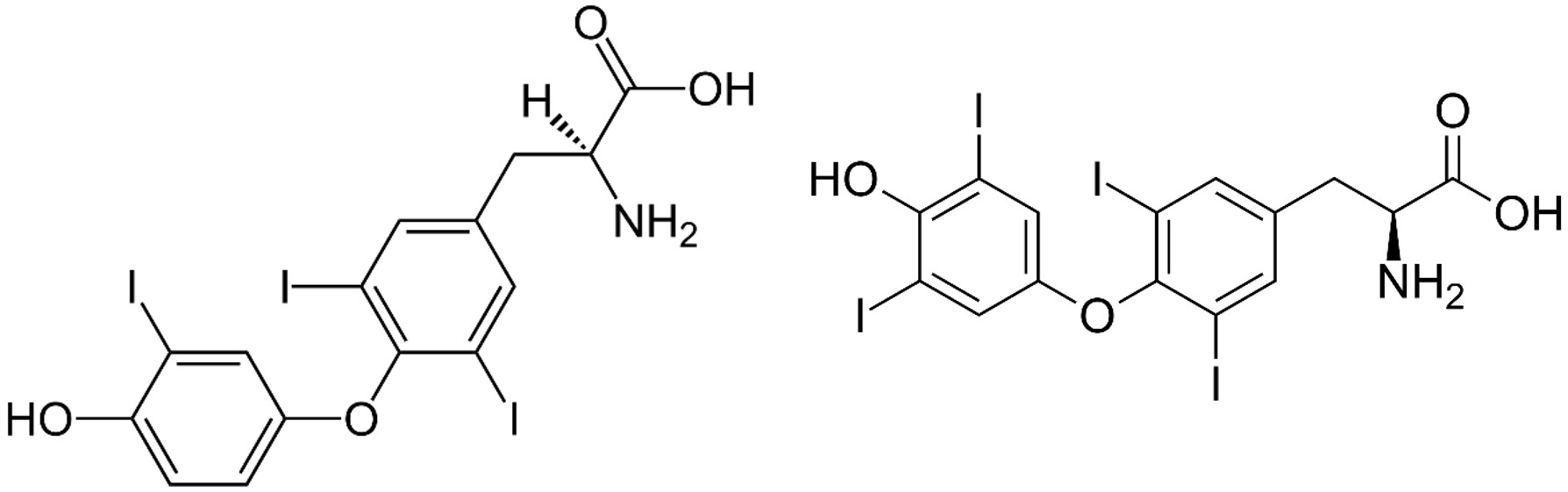
links: wenig aktives Thyroxin (T4), rechts: aktives Triiodthyronin (T3)
Bedeutend sind die Schilddrüsenhormone vor allem auch für Wachstum und Reifung von Ungeborenen im Mutterleib. Bis zum zweiten Schwangerschaftsdrittel ist der Fötus auf die Schilddrüsenhormonversorgung der Mutter abhängig5, sodass eine Störung der Schilddrüsenfunktion mütterlicherseits, z.B. auch durch Umweltfaktoren (sogenannte endokrine Disruptoren), dem Ungeborenen großen Schaden zufügen kann. Dies kann sich z.B. in Verzögerungen in Wachstum und Entwicklung äußern6. Das Wissenschaftlerteam hat daher die Aktivität der Deiodinasen als wichtiges Untersuchungsziel für das Screening von Verbindungen auf Störungen des Schilddrüsenhormon-Systems gefunden.
Die Forscherinnen und Forscher haben einen DIO2-Assay entwickelt, der auf der Sandell-Kolthoff-Reaktion basiert. Der Assay kommt ohne herkömmliche radioaktive Hilfsmittel aus. Mit ihm lassen sich Substanzen bestimmen, die die Deiodinase-Aktivität (in diesem Fall DIO2) hemmen oder fördern und somit das wichtige Gleichgewicht des empfindlichen Schilddrüsenhormonmechanismus stören3.
Im Test werden in einem vorbereiteten Reaktionsgemisch gelb gefärbte Cerium4+-Ionen zu ungefärbtem Cerium-3+-Ionen mit Hilfe von Arsen3+-Ionen reduziert. Iodid wurde zuvor mittels rekombinanter humaner Deiodinase 2 (DIO2) unter Zugabe von Thyroxin (T4) und ggf. den zu testenden Substanzen freigesetzt.3 Die Reaktionsgeschwindigkeit wird in Abhängigkeit von der vorhandenen Iodid-Konzentration erhöht. Die Menge kann so mit Hilfe eines Photometers bestimmt werden.7
Die Sandell-Kolthoff-Reaktion selbst ist ein bekanntes Verfahren und noch heute Grundlage einer WHO-Methode zur indirekten Iodbestimmung.7 Das Wissenschaftlerteam hat den Assay an das 384-Well-Hochdurchsatz-Screening (HTS)-Plattenformat angepasst.
Sechs OECD-Testrichtlinien behandeln Tierversuche mit Ratten, Mäusen oder Kaninchen, die bislang auf irgendeine Weise den Endpunkt Schilddrüsenhormon-wirksame Substanzen integriert hatten. Es sind die Testrichtlinie 414 (Prenatale Entwicklungstoxizitätsstudie), 421 (Reproduktions-/ Entwicklungstoxizitäts-Screeningtest), 422 (Kombinierte Langzeit-Toxizitätsstudie in Kombination mit einem Reproduktions-/Entwicklungstoxizitäts-Screeningtest), 440 (Uterotrophic Bioassay in Nagetieren), 441 (Hershberger Assay) sowie 443 (Erweiterte Ein-Generationen-Reproduktionsstudie).8
In Tierstudien werden entweder lediglich Gewicht und pathologische Veränderungen der Schilddrüse festgestellt oder nur die Schilddrüsenhormone (T3, T4 und TSH) bestimmt.8 Humanspezifische, aussagekräftige in vitro-Tests fehlen.9 Die Entwicklung einer in vitro-Teststrategie, die z.B. von den genauen physiologischen Abläufen ausgeht, ist dringend erforderlich. Deshalb hat die Europäische Kommission das Projektkonsortium ATHENA (Assays for the identification of Thyroid Hormone axis-disrupting chemicals: Elaborating Novel Assessment strategies) aufgelegt,10, 11 mit dem durch die Entwicklung neuer Methoden kritische Lücken bei den Testmethoden für Chemikalien geschlossen werden sollen, die die Schilddrüsenhormonachse stören. Es sollen auch neue Endpunkte für die Ermittlung der nachgeschalteten Auswirkungen auf das sich entwickelnde Gehirn im fötalen und postnatalen Leben festgelegt werden5.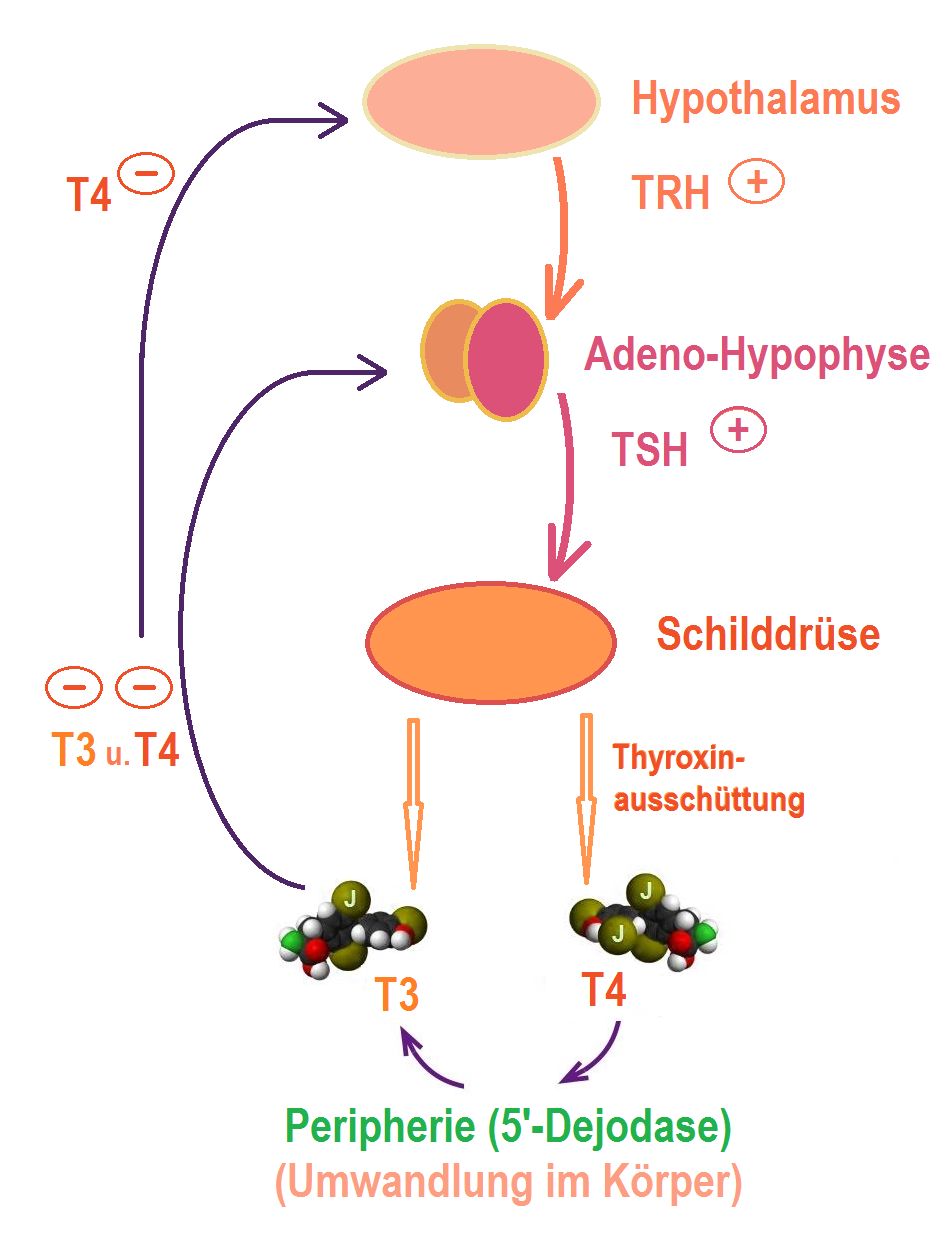
Schildrüsenhormonachse.
Grafik: Geo-Science-International, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=47357720
Das Projekt wird vom EU-Förderkonsortium ATHENA gefördert10, 11. Hier werden neue Methoden entwickelt, die die Folgen des mütterlichen Schilddrüsenhormonmangels auf das sich entwickelnde Gehirn erfassen können.
Der Tierschutzforschungspreis wird alle zwei Jahre vom Landesamt für Gesundheit und Soziales und dem Verband der forschenden Pharma-Unternehmen (vfa) ausgelobt. Das Preisgeld beträgt 30.000 Euro. Er wird am 9. Dezember zwischen 10 und 11 Uhr verliehen2. Aufgrund der aktuellen Coronalage kann die Preisverleihung mit anschließendem Vortrag lediglich über YouTube verfolgt werden: https://www.youtube.com/watch?v=XkLSiDlhtLA
Weitere Informationen:
1 https://expendo.charite.de/
2 https://www.berlin.de/lageso/gesundheit/veterinaerwesen/tierschutz/alternativmethoden/#einladung
3 Caroline Frädrich, Kostja Renko, Niklas Wiese, Anja Fischbach, Carola Seyffarth, Martin Neuenschwander, Jens Peter von Kries & Josef Köhrle (2021). A semi-automatic, non-radioactive 384-well high throughput screening DIO2 assay. Endocrine Abstracts (2021) 73 PEP10.1 | DOI: 10.1530/endoabs.73.PEP10.1
4 https://www.deutsches-schilddruesenzentrum.de/wissenswertes/funktion-der-schilddruese/
5 https://www.deutsches-schilddruesenzentrum.de/wissenswertes/schilddruese-und-schwangerschaft/
6 https://www.forum-schilddruese.de/service/schilddruese-news/schilddruese-news-2012/news-2012-03
7 https://link.springer.com/chapter/10.1007/978-3-662-48986-4_2732
8 https://www.oecd-ilibrary.org/environment/oecd-guidelines-for-the-testing-of-chemicals-section-4-health-effects_20745788
9 Kortenkamp, A., Marta Axelstad, M., Baig, A. H. et al. (2020). Removing Critical Gaps in Chemical Test Methods by Developing New Assays for the Identification of Thyroid Hormone System-Disrupting Chemicals—The ATHENA Project. Int. J. Mol. Sci. 2020, 21, 3123; doi:10.3390/ijms21093123
10 https://cordis.europa.eu/programme/id/H2020_SC1-BHC-27-2018
11 https://cordis.europa.eu/project/id/825161




 Dr. rer. nat.
Dr. rer. nat. Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.
Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.