Der Tierschutzforschungspreis des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz (BMELV) wird für wissenschaftliche Arbeiten, die einen Beitrag insbesondere zur Weiterentwicklung pharmakologisch-toxikologischer Untersuchungsverfahren leisten, vergeben.
Mit seinem Team hat Dr. Landsiedel drei integrierte Testsysteme zur Prüfung der lokalen Toxizität (Reizung von Augen und Haut sowie Hautsensibilisierung) entwickelt bzw. mitentwickelt, wofür er heute den Preis in Empfang nimmt. Sogenannte integrierte Teststrategien sind Ansätze, die verschiedene Datentypen und Informationen in die Entscheidung-erzeugenden Prozesse integrieren. Zusätzlich zu Informationen aus Einzeltests und/oder Testbatterien (also abgestuft ablaufenden Testsystemen) können integrierte Teststrategien auch Ansätze wie die sogenannten "weight-of-evidence" und Expositions-/Populationsdaten in die letztendliche Risikobewertung einer Substanz mit einfließen lassen1.

Diesjährige Forschungspreisträger (von links nach rechts): Dr. Peter Bleser, Staatssekretär des BMELV, Dr. Robert Landsiedel, Dr. Susanne Kolle, Dr. Caroline Bauch, Prof. Dr. Ben van Raventzwaay.
Foto: Günter Friedmann-Marohn, BfR
Eine Überprüfung der lokalen Reizung und Sensibilisierung von Haut und Augen ist bei der Sicherheitsbewertung von Chemikalien im Rahmen der europäischen REACh-Verordnung ab einer Chemikalienproduktion von einer Tonne pro Jahr immer durchzuführen, spielt aber auch z. B. bei der Herstellung von Pflanzenschutz-mitteln oder Kosmetika eine Rolle. BASF hat insgesamt sieben Methoden auf dem Gebiet der Augenreizwirkung, der Hautätz- und Hautreizwirkung sowie der Hautsensibilisierung entwickelt oder mitentwickelt. Einige der Verfahren sind bereits in die OECD-Testguidelines aufgenommen werden, für die übrigen steht dies derzeit noch aus. BASF hat die Methoden in sogenannte Teststrategien eingebaut und nutzt sie in der Routineprüfung von Chemikalien: Bereits 2009 wurde das Labor für Augen- und Hauttoxizität auf Alternativmethoden umgestellt; seit 2012 arbeitet es völlig ohne Tierversuche.
In vitro-tests auf Hautreizwirkung
Hier sind inzwischen zwei Tests in den OECD-Testguidelines anerkannt, der in vitro-Korrosions-test (OECD 431) und der in vitro-Irritationstest (OECD 439). Die Tests basieren auf der Anwendung dreidimensional rekonstruierter Hautmodelle. An der Validierung dieser Methoden war BASF beteiligt.
In vitro-Tests auf Reizwirkung am Auge
Zur Prüfung starker Augenreizwirkungen kann der Bovine Cornea Opacity and Permeability Test (BCOP-Test; OECD 437) eingesetzt werden. BASF war an der Weiterentwicklung und Implementierung dieser Methode maßgeblich beteiligt. Das hierfür benötigte Messgerät, ein Opacitometer, war nicht kommerziell verfügbar. Um den weltweiten Einsatz dieser tierversuchs-freien Methode zu ermöglichen, hat BASF ein Gerät entwickelt und stellt es anderen Labors zum Selbstkostenpreis zur Verfügung.
Während der BCOP starke Augenreizwirkungen erfasst, können schwächere Augenreizwirkungen an humanen dreidimensionalen Hornhautmodellen getestet werden. Dieser Test wird bereits bei der BASF eingesetzt, sodass hier vollständig auf den Draize Test am Kaninchen verzichtet werden kann.
Neben dem BCOP gibt es noch einen weiteren Test, der ebenfalls als Alternative zum Kaninchen-einsatz genutzt werden kann: der Isolated Chicken Eye Test (ICE (OECD 438) mit Augen von geschlachteten Hühnern. Zudem gibt es den HCE (Human Corneal Epithelium-Test) und den HET-CAM Test mit bebrüteten Hühnereiern. Allerdings sind beide Tests noch nicht regulatorisch anerkannt.
Hautsensibilisierung
Untersucht wird das allergene Potenzial einer Substanz. Allergien werden in verschiedenen Typen unterschieden. Im Falle der Hautsensibilisierung sprechen die Forscher vom Allergietyp 4, der erst nach 12 bis 72 Stunden nach Kontakt der Haut mit der Testsubstanz auftritt. Der Allergie liegt eine immunologisch vermittelte Reaktion zu Grunde. Personen erwerben eine solche Allergie oft gegenüber Konservierungsmitteln, Parfüminhaltsstoffen, Farbstoffen oder Nickel- bzw. Chrom-verbindungen. Es können aber auch Allergien gegenüber Inhaltsstoffen aus Putzmitteln und anderen Verbraucherprodukten auftreten. Eine einmal erworbene Allergie auf diesen Stoff bleibt in der Regel ein Leben lang bestehen.
Bislang werden die Tests noch an Tieren durchgeführt mit dem Ziel, das sensibilisierende Potenzial festzustellen. Dazu werden traditionell Meerschweinchen eingesetzt (Guinea Pig Maximization Test GMPT, OECD 406) bzw. der Bühler-Test (OECD 406). Beim Guinea Pig Maximization Test wird den Tieren die Haut geschoren und diese mit der Substanz sowie zusätzlichen Wirkverstärkern für einen bestimmten Zeitraum intra- oder pericutan behandelt. Nach einer bestimmten Inkubationszeit bewerten die Forscher eine Hautrötung und/oder -schwellung, die durch eine allergische bzw. Entzündungsreaktion zustande kommt. ![]()
Zur Zeit noch eine der bevorzugten Spezies in Hautsensibilisierungstests: Guinea Pigs.
Foto: StHuhn, Pixelio.
Im Sinne des 3R Konzeptes ist der Local Lymph Node Assay an Mäusen (LLNA, OECD 429) eine verfeinerte Alternative zu den Meerschweinchentests. Verwendung finden weniger Tiere, die auch weniger belastet werden. Das Verfahren untersucht die immunologische Reaktion im Lymphknoten des Tieres. Das Verfahren ist aber dennoch invasiv: es beruht auf dem Prinzip, dass sensibilisierende Stoffe eine primäre Lymphozytenproliferation (Zunahme der Zellteilung von Lymphozyten) im Lymphknoten auslösen. Nach lokaler Behandlung der Tiere mit der Testsubstanz hinter den Ohren wird die Proliferation der lymphozyten in der Regel mit radioaktiv-markierten Markersubstanzen gemessen, die zuvor über die Schwanzvene injiziert worden sind.
Auch der Mensch kann in die Testreihe miteingegliedert werden: beim Human Repeat Insult Patch Test (HPRIPT) wird Freiwilligen die Substanz in mehreren Wiederholungen und in bestimmten zeitlichen Abständen auf den Rücken aufgebracht und mit Pflastern abgedeckt. Der Test ist aber als ethisch umstritten.
Welche Eigenschaften muss nun ein derartiger Test mitbringen?
Er muss das sensibilisierende Potenzial einer Chemikalie identifizieren können. Für Classification und Labelling der Substanz ist dies ausreichend (EU- Kennzeichnungssystem CLP zur Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen). Für eine vollständige Risiko-bewertung muss jedoch auch die Potenz ermittelt werden können. Hautsensiilisierung ist ein komplexer Prozess; ein einzelner Test kann das nicht abdecken, sondern vielmehr muss ein integriertes Testsystem aus einzelnen Bausteinen genutzt werden, bei dem mehrere in vitro-Tests die unterschiedlichen Aspekte der Sensibilisierung abbilden können.
Bereits 2010 wurden mehrere Tests entwickelt, jedoch reichten die Daten aus einem Einzeltest für die Risikobewertung einer Substanz nicht aus. Daher haben die Forscher um Dr. Landsiedel eine Testkombination entwickelt, die in verschiedenen europäischern Labors auf ihre Zuverlässigkeit, Übertragbarkeit und Reproduzierbarkeit hin getestet worden ist.
Das Testsystem besteht aus drei Tests, dem Direct Peptide Reactivity Assay (DPRA), dem human Cell Line Activation Test (h-CLAT), bestehend aus einer humanen Zelllinie, sowie einem Keratinozyten-Aktivierungsassay (dem KeratinoSensTM oder dem von der BASF entwickelten Lizenz-freien LuSens-Assay).
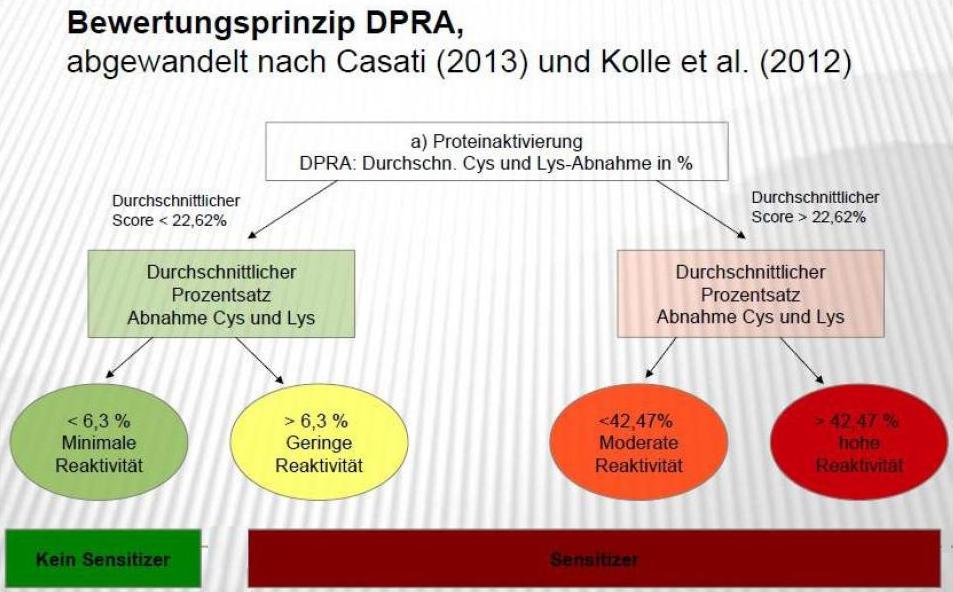
1. Direct Peptide Reactivity Assay (DPRA)
Niedermolekulare Substanzen sind selbst zu klein, um allergen zu wirken. Sie müssen mit körpereigenen Proteinen zunächst einen Komplex bilden. Dieser sich im Körper abspielende Mechanismus wird im Direct Peptide Reactivity Assay (DPRA) abgebildet. Synthetische Peptide, die Cystein und Lysin-Bindestellen besitzen, simulieren dabei die körpereigenen Proteine. Durch die Bindung der Testsubstanz nimmt die Konzentration der synthetischen Peptide ab. Die Abnahme des Peptides wird analytisch gemessen und dient als Maß für die Reaktion der Testsubstanz mit den körpereigenen Proteinen.
2. Human Cell Line Activation Test (hCLAT)
Hier wird die Aktivierung von Zellen in Kultur gemessen. Die verwendeten Monozyten sind Vorläufer für einen bestimmten Immunzelltyp der Epidermis der Haut (Langerhans-Zellen). Nach Exposition mit der Testsubstanz werden Oberflächenproteine (CD86, CD54) auf den Zellen überprüft und deren Menge durchfluss-zytometrisch gemessen.
3. Keratinozyten-Aktivierungsassays
Der dritte Test untersucht einen bestimmten Signalweg in den Zellen. Genutzt werden immortalisierte humane Keratinozyten (spezialisierte Zellen der menschlichen Epidermis). Das Prinzip basiert darauf, dass die meisten Allergene eine bestimmten Signalweg aktivieren, den Nrf2-Keap1-ARE-Signalweg. In die Keratinozyten ist ein Reportergenkonstrukt eingebaut worden mit dem Ziel, eine Signalwegaktivierung nach Exposition mit der Testsubstanz luminometrisch erkennen zu können. (Eingebaut wurde ein Luziferasegen unter der Transkriptionskontrolle des Antioxidant Response Elements (ARE)).
InVitroJobs sprach kurz vor der Preisverleihung mit dem Preisträger Dr. Robert Landsiedel.
InVitroJobs:
Wir möchten Ihnen und Ihrem Team natürlich herzlich gratulieren.
InVitroJobs:
Wie fühlen Sie sich heute mit der Anerkennung?
Dr. Landsiedel:
Das gesamte Team freut sich sehr über diese Anerkennung. Der größte Erfolg ist sicher, dass wir durch langjährige pragmatische Entwicklungsarbeit tatsächlich eine ganze Gruppe von Effekten – die gesamte lokale Toxizität – vollständig ohne Tierversuche prüfen können. Und das auch tatsächlich in der Routineprüfung von Chemikalien umgesetzt haben. Das wird mit dem heutigen Preis noch einmal sehr sichtbar anerkannt.
InVitroJobs:
Mit Ihren Alternativlaboren sind Sie ja in eine Vielzahl an Ersatzverfahrenentwicklungen involviert: Für welche ihrer Entwicklungen bekommen Sie denn heute den Preis? Können Sie das näher spezifizieren?
Dr. Landsiedel:
Für die Entwicklung mehrerer Methoden, die wir zum Teil in Teststrategien zusammengeführt haben und so alle Endpunkte der lokalen Toxizität ohne Tierversuche abprüfen können. Also: Hautreizwirkung, Hautätzwirkung, Augenreizwirkung und Hautsensibilisierung.
InVitroJobs:
Wird der bereits validierte BCOP-Test also der Bovine Cornea Opacity and Permeability Test als Ersatz zum Kaninchenaugenreizungstest schon flächendeckend eingesetzt? Es gibt doch immer noch Firmen, die den Kaninchenaugenreizungstest durchführen und, soweit ich gelesen habe, gilt er auch nicht als vollständiger Ersatz zum Augenreizungstest. Woran liegt das denn? Braucht man da mehrere Tests?
Dr. Landsiedel:
Der BCOP wurde von der OECD in eine Testguideline (Nr. 437) gefasst. Mit dem Test können starke Augenreizwirkungen erkannt werden. Im Sommer dieses Jahres wurde die Testguideline überarbeitet und nun ist es auch möglich, jegliche Reizwirkungen am Augen mit dem BCOP auszuschließen. Für den Bereich zwischen keiner und starker Reizwirkung am Auge – also die nicht-starke Reizwirkung - nutzen wir bei der BASF ein Corneamodell aus Humanzellen, EpiOcular.
Und es gibt Substanzen - viele Formulierungen zum Beispiel - die nicht im BCOP getestet werden können. Hier gibt es noch Bedarf zur weiteren Anpassung der Methoden.
InVitroJobs:
Die internationale Nachfrage nach Ihrem Opacitometer war ja groß und hat in der Presse Beachtung gefunden: Setzen auch die Chinesen das Gerät mittlerweile ein?
Dr. Landsiedel:
Wir haben bisher etwa 20 Geräte ausgeliefert. Parallel dazu werden die Labors geschult, um den BCOP korrekt durchführen zu können. Diese Schulungen führt unser Partner in den USA, das Institute for In Vitro Science (IIVS), durch. Wir hatten auch Schulungen in China; ob und wie der BCOP in China heute schon eingesetzt wird, kann ich nicht sagen.
InVitroJobs:
Wie lange hat es gedauert, bis Sie das ITS soweit entwickelt hatten, dass sie es bei der ECVAM einreichen konnten?
Dr. Landsiedel:
Für die Teststrategie zur Hautsensibilisierung haben wir insgesamt 14 Methoden getestet und letztlich vier Methoden als geeignet ausgewählt. Mit drei dieser Methoden haben wir eine Teststrategie entwickelt, die die Hautsensibilisierung beim Menschen ebenso gut vorhersagt wie der Local Lymph Node Assay (LLNA), der bisherige ‚Standard‘ Tierversuch. Die Entwicklung bei uns hat etwa fünf Jahre gedauert. Hinzu kommen die Arbeiten, die externe Partner in die Methoden investiert
haben, auf denen unsere Strategie aufbaut.
InVitroJobs:
Wie lange wird die Anerkennung bzw. die Aufnahme in die OECD-Testguidelines noch dauern?
Dr. Landsiedel:
Dazu kann ich nichts sagen. Nach dem Stand der Entwicklung und Validierung der Methoden rechne und hoffe ich, dass dies 2014 geschieht. Die Teststrategie haben wir ebenfalls zur Validierung bei ECVAM eingereicht. ECVAM hat allerdings erst für 2016 eine Teststrategie angekündigt. Das ist für die allermeisten Substanzen unter REACH sehr spät.
InVitroJobs:
Woran tüfteln Sie denn im Moment?
Dr. Landsiedel:
Bei der Hautsensibilisierung arbeiten wir zur Zeit an zwei Fragestellungen: Wie können wir nicht nur sagen, ob eine Substanz hautsensibilisierend ist, sondern auch wie stark die Sensibilisierungspotenz ist? Und zweitens: Wie können wir Substanzen testen, die sich nicht im Zellkulturmedium lösen lassen? Darüber hinaus beschäftigen uns schon seit langem die komplexeren toxikologischen Endpunkte: Reprotox und systemische Toxizität. Dies wird unser Schwerpunkt für die kommenden Jahre sein.
InVitroJobs:
Wir danken recht herzlich für das Gespräch.
1 Integrated Testing Strategies & Risk Assessment. (http://www.alttox.org/ttrc/emerging-technologies/its/)




 Dr. rer. nat.
Dr. rer. nat. Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.
Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.