Arbeitsgruppe im Portrait: Aachener Centrum für
Technologietransfer in der Ophthalmologie (ACTO) e.V.
ACTO ist ein An-Institut der Rheinisch-Westfälischen Technischen Hochschule Aachen (RWTH), d.h. eine organisatorisch, finanziell und rechtlich unabhängige wissenschaftliche Einrichtung, die trotzdem einer Universität angegliedert ist. Dadurch ist die Innovation weniger durch Bürokratie beeinträchtigt. Das Aachener Centrum für Technologietransfer in der Ophthalmologie wurde 1998 gegründet. Es arbeitet an der Schnittstelle zwischen Grundlagen- und angewandter Forschung. Leitziel von ACTO ist die interdisziplinäre Wissenschaftskooperation zwischen Ärzten, Grundlagenwissenschaftlern, Technikern, Biologen, Informatikern und Ingenieuren sowie die Verzahnung von Grundlagen- und Anwendungsforschung in der Augenheilkunde. Die Forschungsschwerpunkte bestehen in der Entwicklung künstlicher Hornhautimplantate und in der tierversuchsfreien Testung von Chemikalien an der Hornhaut (Cornea). Zudem werden neue Grundlagen für die Verträglichkeit von Augentropfen erforscht und ein Online-Sehtest entwickelt. Um diese Aufgaben bewältigen zu können, unterhält ACTO Forschungslabore sowohl in Köln als auch in Aachen.
Menschliches Auge mit Cornea-Implantat nach einer Woche.
Foto: ACTO
Vorsitzender von ACTO ist Prof. Dr. med. Dr. h.c. Norbert Schrage. Er ist seit 2004 Chefarzt der Augenklinik Köln-Merheim und war zuvor kommissarischer Direktor der Universitätsaugenklinik Aachen (1). Stellvertretender Vorsitzender ist Univ.-Prof. Dr. med. Peter Walter, Direktor der Augenklinik des Universitätsklinikums Aachen. Vor Kurzem wurde Prof. Schrage von der Pirogov Universität Moskau mit der Ehrendoktorwürde „für die Forschungsleistung auf dem Gebiet der Entwicklung von Hornhautprothesen und zur Erforschung der Therapie der Verätzung des Auges“ geehrt (2).
Ex Vivo Eye Irritation Test (EVEIT)
ACTO hat ein Ersatzverfahren für den sehr umstrittenen, da unter anderem wenig prädiktiven und schmerzhaften Draize-Test am Auge eines lebenden Kaninchens entwickelt. Das Verfahren stellt – ähnlich dem Bovine Corneal Opacity/Permeability Assay1 (BCOP) – eine tierversuchsfreie Alternative zum Draize-Test auf Augenreizung am lebenden Kaninchen dar. Wesentliches Kriterium des Ersatzverfahrens zum Tierversuch EVEIT ist die Möglichkeit, außerhalb eines Tierversuches dynamisch die Heilung von Wunden unter exakt reproduzierbaren Versuchsbedingungen zu beobachten (3). Dabei ist es den Forschern gelungen, Hornhäute von geschlachteten Kaninchen über 28 Tage in Kammern zu kultivieren und dabei den Stoffwechsel der Zellen stabil zu halten. Die Testchemikalie wird dann auf die Hornhautkultur aufgegeben. Hiernach können geschädigte Bereiche mit verschiedenen Methoden untersucht werden. Umgekehrt kann auch der Heilungsverlauf künstlich geschädigter Hornhautkultur in vitro untersucht werden, nachdem z.B. ein neues Augenarzneimittel auf die Kultur aufgegeben worden ist. Mit dem Test können auch wiederholte Substanzanwendungen bis zu 100 Mal am Tag getestet werden.

Hornhaut in der EVEIT-Kammer.
Foto: ACTO.
Bei der in vitro-Prüfung der akuten Augenreizung werden Hornhauttrübungen und Veränderungen der oberflächlichen und tieferen Hornhautschichten mit vier Methoden untersucht: mit dem Mikroskop, der Optischen Kohärenztomografien (OCT)2, biochemisch und histologisch - also weitaus genauer als es beim Kaninchen der Fall ist. In einem seitens des Bundesministeriums für Bildung und Forschung geförderten Projektes wurde in Kooperation mit dem Institut für Halbleitertechnik an der RWTH Aachen (IHT) und der Innolabtec GmbH gezeigt, dass der EVEIT in Kombination mit der OCT-Technik durchaus mit den Ergebnissen der Tierversuche mithalten kann. Für diese Entwicklung wurde Dr. Spöler (IHT) im Jahre 2010 von der „Europäischen Partnerschaft für alternative Methoden zu Tierversuchen“ (EPAA) mit dem Wissenschaftspreis ausgezeichnet (1).

Kontrolle der Heilung einer Hornhaut mit vier verletzten Stellen mit Hilfe von Fluoreszein3 und Blaulicht.
Fotos: ACTO
Optischer Kohärenztomograf
Bei der OCT wird Licht geringer Kohärenzlänge zur Entfernungsmessung streuender Materialien eingesetzt. Das Untersuchungsobjekt wird punktweise abgetastet. Der Haupteinsatz liegt derzeit hauptsächlich bei der Untersuchung des Augenhintergrundes bzw. des hinteren Augenabschnittes. Das Verfahren ermöglicht eine hohe Eindringtiefe des Lichts in das Gewebe (bis zu 3 Millimeter). Auflösung und Messgeschwindigkeit sind vergleichsweise hoch.
Kohärenzlänge ist ein Begriff aus der Optik und bezeichnet einen maximalen Weglängen- oder Laufzeitunterschied, den zwei Lichtstrahlen aus derselben Quelle haben dürfen, damit bei ihrer Lichtwellenüberlagerung noch ein (räumlich und zeitlich) stabiles Interferenzmuster entsteht. Die Interferenz ist die Änderung der Amplitude bei der Überlagerung von zwei oder mehr Wellen durch Addition ihrer Auslenkungen.
Durch eine Testsubstanz im in vitro-Versuch kann die untersuchte Cornea schrumpfen. Diese Abnahme der Schichtdicke wird im Kohärenztomografen als Zunahme der Signalamplitude angezeigt (4).
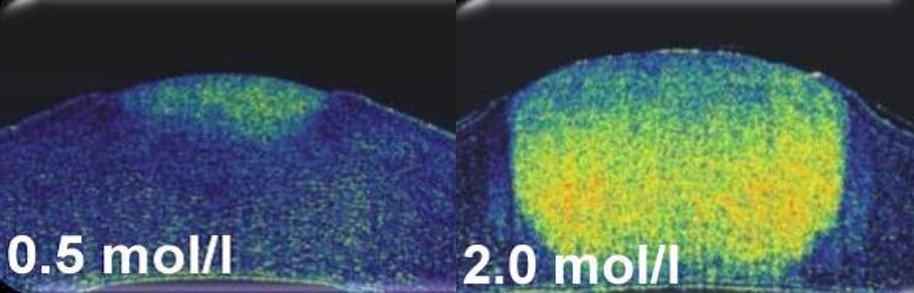
Nachweis der Tiefe der Verletzung mit Natronlauge (NaOH) bei gleichen Einwirkzeiten und mit verschiedenen Konzentrationen mit Hilfe der Optischen Kohärenztomografie (OCT).
Fotos: ACTO.

Versuchsaufbau im Brutschrank.
Foto: ACTO.
Äußerst schmerzhaft und veraltet: Der Draize-Test
Der amerikanische Toxikologe John Henry Draize hat den nach ihm benannten Draize-Test am Kaninchenauge bereits Anfang der 40er Jahre zur Prüfung einer möglichen reizenden Wirkung von Testchemikalien wie z.B. Kosmetika oder Industriechemikalien entwickelt. Dabei wird lebenden Kaninchen die Substanz auf die Hornhaut des Auges aufgetragen und Tage oder sogar Wochen abgewartet, ob sich Hornhauttrübungen / -verletzungen bzw. Bindehautentzündungen ergeben. Heutzutage wird der Kaninchentest dann durchgeführt, wenn in vitro-Alternativen bereits getestet worden sind und in den Resultaten kein reizendes Potenzial der Substanz gefunden wurde. Die OECD empfiehlt, bei der Untersuchung einer akuten Augenätzung oder -reizung eine integrierte Teststrategie durchzuführen und erst einen Tierversuch in Erwägung zu ziehen, wenn es angemessen und notwendig ist, d.h., wenn alle anderen Maßnahmen wie weight-of-evidence4-Analysen der bereits vorhandenen Daten sowie validierte und akzeptierte in vitro Tests, bzw. alle verfügbaren Alternativmethoden realisiert worden sind. Dabei wird die Substanz den Tieren in den Bindehautsack geträufelt (OECD-Testrichtlinie Nr. 405 vom Oktober 2012, (5)).
Der Draizetest am Kaninchen ist sehr umstritten. Trotzdem ist er bislang nicht vollständig ersetzt worden. Unabhängig von der sehr hohen Belastung für die Tiere - die Schädigung der Horn- und Bindehaut ist äußerst schmerzhaft - gibt es auch zahlreiche Unterschiede zwischen der Hornhaut des Kaninchens und der des Menschen, für dessen Sicherheit die Testergebnisse im Allgemeinen gedacht sind. Forscher sprechen von Zufallsergebnissen, und jedes Labor kann zu anderen Kaninchentestergebnissen kommen.
Hinzu kommen die Artunterschiede, von denen hier nur einige genannt seien (6):
- Das Kaninchenauge ist 10 Mal durchlässiger für wasserlösliche Substanzen als das Menschenauge
- Die Schmerzschwelle beim Kaninchen ist höher als beim Menschen
- die Cornea des Kaninchens ist weitaus dünner als die des Menschen
- Kaninchen haben ein weniger effektives Tränensystem als der Mensch
- Im Gegensatz zum Kaninchen verfügt der Mensch über die Fähigkeit, in Reaktion auf toxische Substanzen im Corneaepithel Vakuolen auszubilden
- der pH der Augenflüssigkeit des Kaninchens ist alkalisch, der des Menschen eher neutral
Soll der Vergangenheit angehören: Kaninchen im Draize-Test
Foto: People for the Ethical Treatment of Animals (PETA)
Seit September 2009 gestattet die OECD verschiedene in vitro-Tests z.B. mit isolierten Rinder-Hornhäuten (aus „Schlachtabfällen“) als Ersatz für die Tests zur Prüfung eines stark reizenden Potenzials (den sogenannten BCOP-Test, OECD-Testrichtlinie 437, (7, 8)). Bei negativem Ausgang des BCOP-Test wird der Draizetest verlangt. Neben dem BCOP-Test gibt es noch weitere Tests, die ebenfalls als Alternative zum Kaninchen genutzt werden können, z.B. der Isolated Chicken Eye Test5 (ICE, OECD-Testrichtlinie 438) mit Augen von geschlachteten Hühnern. Zudem gibt es den Human Corneal Epithelium-Test6 (HCE) und den HET-CAM Test7 mit bebrüteten Hühnereiern. Allerdings sind diese beiden Tests regulatorisch nicht anerkannt (und deshalb nicht einsetzbar). Mehrere Forscher haben sich auch auf die Entwicklung von Cornea-Modellen aus menschlichen Zellen spezialisiert (9, 10, 11, 12, 13). Keiner der Tests konnte den Draize bislang jedoch vollständig ablösen. Deshalb ist es notwendig, weiter Alternativmethoden zu erforschen und zu validieren.
GHS System-Kategorien
Nach einer internationalen Vereinbarung (Globally Harmonized System, GHS) sind Chemikalien in ganz bestimmter Art und Weise zu klassifizieren und zu kennzeichnen. Die Substanz ist dann mit einem (oder mehreren) Symbol und einem Wort zu kennzeichnen. In Bezug auf mögliche Augenschädigungen gibt es drei Kategorien, in die Chemikalien eingeordnet werden können:
Kategorie 1: die Substanz kann ernsthafte Augenschädigungen verursachen
Kategorie 2A: die Substanz kann ernsthafte Augenreizungen verursachen
Kategorie 2B: die Substanz kann Augenreizungen verursachen (14).
Lässt sich humane Cornea mit Stammzellen künstlich herstellen?
Mittlerweile hat die Stammzelltechnik Fortschritte gemacht: vor Kurzem haben amerikanische Forscher in Massachusetts mit Hilfe von Tracermolekülen sogenannte limbale Stammzellen im menschlichen Auge gefunden, mit denen Sie erfolgreich humane Cornea züchten konnten. Das Verfahren wird als vielversprechend angesehen, um zukünftig Patienten mit Augenverletzungen zu heilen (15, 16, 17).
Bei fortschreitender Technik ist es durchaus wahrscheinlich, dass auch induzierte pluripotente Stammzellen es zulassen könnten, im größeren Stil vollständige Augenhornhäute zu entwickeln, die als Ersatzverfahren für Augenätzungs- und -reizungstests eingesetzt werden können. Das in vitro-Okular-Modell von Across Barriers (humanes Corneakonstrukt) beispielsweise besteht aus humanen Hornhautepithelzellen (HCE-T Zelllinie) des Auges und einer humane Hornhaut-Keratinozytenzelllinie (HCK-Ca Zelllinie). Getestet werden heute schon Permeation und Verträglichkeit von Augenarzneimitteln (9, 10, 11, 18).
„…viel sensibler und genauer….“
InVitroJobs führte ein Gespräch mit Prof. Dr. med. Dr. h.c. Norbert Schrage, Gründer und Vorsitzender von ACTO e. V.
InVitroJobs: Können Sie Ihre Innovation kurz beschreiben?
Prof. Schrage: Der von ACTO entwickelte Ex Vivo Eye Irritation Test (EVEIT) soll langfristig den DRAIZE Test und Tierversuche in der Pharmaforschung am Auge ersetzen. Augen von Schlachtkaninchen werden so behandelt, dass sie für einige Wochen kultiviert werden. Damit ist eine Methode verfügbar, die Versuche am lebenden Tier (also Tierversuche) entbehrlich macht und das bei gleichwertiger bzw. sogar deutlich besserer Aussagekraft. Wesentliches Kriterium dieser Methode ist die Heilung von Wunden und chemischen Verletzungen in vitro. Die so an der Hornhaut durchgeführten Versuche dienen dem Ziel, Wirkung, Verträglichkeit und Nebenwirkungen wie z.B. Verkalkungen durch phosphathaltige Augentropfen vor der Anwendung am Menschen zu erkennen.
InVitroJobs: Welche Substanzen kann man mit dem EVEIT testen?
Prof. Schrage: Im EVEIT können sowohl chemische, pharmakologische sowie kosmetische Substanzen/Produkte getestet werden.
InVitroJobs: Welche Bedeutung hat die Technik für den Ersatz des Tierversuchs am Kaninchen?
Prof. Schrage: Das EVEIT System soll die Tierversuche mit Substanzen, Chemikalien oder Medikamenten am Auge vollständig ersetzen. Im Vergleich mit dem Draize-Test konnte ACTO nachweisen, dass der EVEIT viel sensitiver und genauer ist, da die zu untersuchende Substanz viel kontrollierter aufgetragen, die Wirkung beobachtet und abgespült werden kann. Es kann auch zwischen dem mechanischen und chemischen Schaden unterschieden werden, was im Tierversuch immer ein Mischergebnis ist. Der Versuch ist des Weiteren viel schneller und genauer als ein Tierversuch. Ferner kann im EVEIT auch eine verzögert einsetzende Schädigung des Auges nachgewiesen werden.
InVitroJobs: Wie viele Tiere könnte man mit Ihrem Test einsparen?
Prof. Schrage: Im Jahr 2007 wurden in Deutschland Versuche an über 2,6 Millionen Tieren durchgeführt, wovon ca. 17.000 Tierversuche auf organspezifische Untersuchungen von Haut- und Augenreizungen entfallen. Diese Tierversuche könnten durch den EVEIT ersetzt werden.
InVitroJobs: Was unterscheidet Ihren Test von dem Bovine Corneal Opacity/Permeability Assay (BCOP)?
Prof. Schrage: Mit dem BCOP-Test können Chemikalien der Kategorie CAT18 nur im Hinblick auf ihre akute Wirkung getestet werden, das heißt, die Änderung der Durchsichtigkeit, gemessen mit einem für den Augenarzt eher merkwürdigen und schwer zu kalibrierenden Durchlichtverfahren und ferner die Veränderung der Permeabilität für Natrium Fluoreszein. Mit dem EVEIT-System können sowohl diese Verfahren verwendet werden, zusätzlich sehen wir durch die Kulturtechnik aber auch eine Heilung oder auch Nicht-Heilung innerhalb einer definierten Zeit. Damit können die im Kulturmedium gehaltenen und nicht nur mit Chemikalien der Kategorie CAT 1 verätzten Kaninchenhornhäute in Bezug auf die Dauerhaftigkeit eines Schadens, also die essentiell wichtige Frage beantwortet werden: Heilt eine Verletzung aus und wenn ja, gibt es eine Narbe oder eine vollständige Wiederherstellung des gesunden Gewebes. Dies ist für mich als Augenarzt die wesentliche Frage bei meinen im bisherigen Berufsleben gesehenen klinischen 1.500 Verätzungspatienten. Dies macht den entscheidenden, für den Menschen relevanten Unterschied in der Bewertung des EVEIT als klinisch relevanter Test zum BCOP aus.
InVitroJobs: Dreh- und Angelpunkt ist die Heilung von Wunden in vitro: Wie kann man sich das vorstellen?
Prof. Schrage: Im Langzeit-Ex-Vivo-Eye-Irritation-Test (EVEIT-longterm) werden Hornhäute von toten Kaninchen, die aus der Lebensmittel-herstellung stammen, heraus präpariert und in eine künstliche Augenkammer übernommen. In dieser Kammer werden sie durch Kulturmedium ernährt und mikroskopisch überwacht, sodass eine gesunde Hornhaut bis zu 28 Tage in der Kultur lebt. Dieses Verfahren kennen wir aus der medizinischen Anwendung der Hornhautkultur und Transplantation von menschlichen Spenderhornhäuten. Der Zustand der Hornhaut wird anhand von biochemischen Messwerten, der Prüfung auf Klarheit, Stabilität des Epithels (äußere Deckschicht) und Funktionieren des Endothels (innere Deckschicht) überprüft. Erst wenn diese Kriterien erfüllt sind, werden die Hornhäute an Tag 2 bei den reinen Heilungsversuchen mittels eines Zahnschleifers an vier Flächendefinierten verschiedenen Stellen verletzt, anschließend mit der zu testenden Substanz betropft und für 3 bis 20 Tage in einem Brutschrank unter ständiger Zufuhr von Kulturmedium kultiviert. Täglich werden mittels Fluoreszenzangiografie9 und unter Zuhilfenahme der Optischen Kohärenztomografie (OCT) Fotos von den Hornhäuten und den einzelnen verletzten Stellen gemacht und mittels Glukose-Laktat-Bestimmung die Lebensfunktionen der Hornhaut beobachtet. Durch die tägliche Beobachtung kann genau gemessen und gesehen werden, ob und wie schnell eine Heilung der verletzten Stellen an der Hornhaut vonstatten geht. Dies wird digital ausgewertet und in einer Heilungskurve pro Hornhaut im Laborprotokoll festgehalten.
InVitroJobs: Der gängige BCOP wird in der Regel mit weiteren Tests wie CAMVA10 oder HET-CAM, kombiniert. Ist das mit Ihrem Test auch nötig?
Prof. Schrage: Im Rahmen der an den EVEIT gestellten Fragestellungen sind zusätzliche Tests wie CAMVA oder HET-CAM nicht nötig, da diese Antworten auf Fragen der erweiterten Toxizität geben, die bezogen auf das Auge eher unspezifisch sind. Die Hämorrhagien im HET-CAM finden sich vergleichbar als OCT Veränderungen in der Hornhaut wieder. Als ergänzende Parameter dienen uns histologische Färbungen sowie Tests zur Permeabilität und der Vitalitätsnachweis der Hornhaut mittels Glukose-Laktat-Quantifizierung. Insbesondere sind Messungen der Opazität11 und der Permeabilität am lebenden Hornhautmodell direkt möglich. Ferner benutzen wir die deutlich genauer differenzierende Optische Kohärenztomografie zur Untersuchung der Hornhaut.
InVitroJobs: Wie wird denn der Endpunkt12 gemessen/detektiert? Wie wird der Endpunkt Augenätzung leicht - mittel - schwer, Augenreizung leicht - mittel- schwer, nicht reizend klassifiziert? Haben Sie dafür ein Messgerät, an dem man nur einen Wert ablesen muss?
Prof. Schrage: Normalerweise legt der vollständige Heilungsprozess der Negativkontrolle, die in jeder Versuchsreihe mitläuft, den Endpunkt fest. Dafür reichen i.d.R. 3 Versuchstage. Für speziellere Fragestellungen ist ein Beobachtungszeitraum darüber hinaus realisierbar. Eine gewisse Klassifizierung in der Exposition ist z.B. möglich durch variable Applikationsfrequenzen (z.B. stündliche oder 1x tägliche Applikation der Testsubstanz).
Die Endpunkte sind definiert als: Heilung des Epithels im Fluorescein-Test3, Trübung der Hornhaut im durchfallenden Licht, Trübung der Hornhaut in der Optischen Kohärenztomografie inklusive Eindringtiefe der Läsion im OCT, die globale Permeabilität der Hornhaut sowie Glucose-Lactat-Messungen der Hornhaut in Kultur. Endpunkte in der Histologie sowie dynamische Beobachtungen sind wegen des langen Verlaufes der Tests über 3 bis 6 Tage klinisch möglich.
InVitroJobs: Nach unseren Informationen setzt man in Europa bislang noch das Kaninchen ein, wenn sich das Augenreiztestergebnis als negativ herausgestellt hat, also um sicherzugehen, dass nicht noch sehr leichte Reizungen auftreten, die man mit dem BCOP und den anderen Tests nicht detektiert hat. Wie ist das mit Ihrem Test?
Prof. Schrage: Unserer Meinung nach kann mit unserem Test die Schwelle einer Reizung sehr genau bestimmt werden, da wir im Gegensatz zu den bisherigen Verfahren nicht einmal, sondern auch mehrfach tropfen können. So haben wir im Einmal-Test völlig unbedenklich getestete Substanzen bei der Erhöhung der Tropffrequenz als epithelheilungsstörend oder sogar toxisch sehen können. Ein gutes Beispiel sind die von uns veröffentlichten Arbeiten zu den klassischen Konservierungsmitteln in der Augenheilkunde wie Benzalkoniumchlorid oder Purite®.
(Zitat: The Ex Vivo Eye Irritation Test (EVEIT) in evaluation of artificial tears: Purite-preserved versus unpreserved eye drops. Schrage N, Frentz M, Spoeler F. Graefes Arch Clin Exp Ophthalmol. 2012 Sep;250(9):1333-40. doi: 10.1007/s00417-012-1999-3. Epub 2012 May 15).
Hier zeigte sich in der Einmalapplikation keine Toxizität. Jedoch bei stündlicher Applikation war nach 3 Tagen eine erhebliche Epithelheilungsstörung oder irreversible Degeneration detektierbar. Dies deckt sich mit den klinischen Ergebnissen bei Patienten, die auf konservierte Medikamente bei hohen Tropffrequenzen mit toxischen Nebenwirkungen kämpfen. Dies bedeutet, dass mit Hilfe des EVEIT-Systems ein Titrieren (Einstellen) der Maximaldosis möglich wird. Damit ist eine extrem genaue Differenzierung des Begriffes toxisch möglich, wie dies im Tierversuch nie erreichbar ist, aber am Menschen typischerweise auftritt. Der Satz des Paracelsus, dass die Dosis das Gift macht, ist hier aktuell wie nie. Was für eine unsinnige Vorgehensweise es ist, eine hoch konzentrierte Substanz auf das Auge zu geben und zu meinen, damit die Toxizität messen zu können. Dies lässt sich an einem einfachen Beispiel, das ich nicht zum Selbstversuch empfehlen möchte, verdeutlichen: schütten Sie mal einige Körner Kochsalz in den Bindehautsack des Auges und beschreiben Sie die Wirkung von Kochsalz. Sie werden konkret merken, wie irritierend (ätzend) toxisch dieses Lebensmittel in dieser Form angewendet ist. Es ist daher zu fordern, dass Grenzwerte der Einmal- und wiederholten Anwendung definiert werden. Dazu eignet sich der EVEIT-Test ganz besonders. Mit diesem Test wurden bereits mehrere Tränenersatzstoffe und neue Medikamente getestet und durch die benannten Stellen des BfARM13 zugelassen.
(Zitat: Semifluorinated alkanes as a liquid drug carrier system for topical ocular drug delivery. Dutescu RM, Panfil C, Merkel OM, Schrage N. Eur J Pharm Biopharm. 2014 May 15. pii: S0939-6411(14)00158-1. doi: 10.1016/j.ejpb.2014.05.009)
InVitroJobs: Inwieweit besteht ein Unterschied zwischen humaner Cornea und der Cornea vom Tier?
Prof. Schrage: Die Kaninchenhornhaut ist die Hornhaut eines Jungtiers, dies ist insofern mit Kinderhornhäuten vergleichbar, nicht mit der eines Erwachsenen. Insofern sind diese Hornhäute deutlich permeabler und dünner und reagieren somit auch heftiger als die humane erwachsene Hornhaut. Damit sind diese Tests in Bezug von Safety (im Sinne der Risikobewertung durch ihre höhere Sensibilität) auf der richtigen Seite angesiedelt und eher zu sensibel.
InVitroJobs: Wie sind die Aussichten, Ihr Verfahren im Hochdurchsatzverfahren einzusetzen?
Prof. Schrage: Wir entwickeln gerade Modifikationen unseres Systems, um Hindernisse in der Kulturtechnik, Fehlerstellen und hohe Anforderungen an Handling und Applikation zu vereinheitlichen und vor allem zu vereinfachen. Es existiert ein geprüftes SOP14, das dann modifiziert wird. Wir wollen unser Verfahren durch die Europäische Kommission (ECVAM15) in eine Prävalidierung (19) bringen und gleichzeitig ohne Veränderung der eigentlichen Kulturbedingungen ein Hochdurchsatzverfahren etablieren und gemeinsam mit anderen Partnern in Interlaborversuchen validieren. Da die Kaninchen kommerziell für die Schlachtung im 100.000er-Maßstab in Deutschland gezüchtet werden und hier eine extrem hohe Standardisierung der Tierhaltung und genetische Einheitlichkeit vorliegen, ist uns um Nachschub an Kaninchenaugen nicht bange.
InVitroJobs: Könnte man aus ethischen Gründen in Ihrem Test später auch einmal humane Cornea, die aus der Zellkultur entwickelt wurde, einsetzen?
Prof. Schrage: Ja, wenn es sich um Spenderhornhäute handelt, die nicht zur Transplantation geeignet sind, könnte man in unserem Test auch menschliche Hornhäute einsetzen. Dies bedarf der Einwilligung des Spenders oder seiner Angehörigen. Dazu wird die EVEIT-Kammer derzeit weiter entwickelt, da die Kaninchenhornhaut etwas kleiner ist als die menschliche Hornhaut. Da die Kulturtechnik dann auch gleich starten müsste, sind dazu erhebliche arzneimittelrechtliche Auflagen zu erfüllen, die durch die aktuelle Gesetzgebung eine solche Entwicklung sehr schwierig machen. Dazu gehört ja auch, dass nicht immer direkt bekannt ist, ob eine Hornhaut zur Transplantation geeignet ist oder nicht. Die nicht zu verwendende menschliche Spenderhornhaut wird durch das heutige Kulturverfahren so verändert, dass eine EVEIT-Kultur nicht mehr sinnvoll möglich ist. Daher wäre eine Umstellung der Inkulturnahme notwendig, was derzeit von einem kleinen Institut ohne externe Hilfe durch großzügige Spenden nicht realisiert werden kann.
InVitroJobs: In welcher Testphase befindet sich Ihr Test?
Prof. Schrage: Wir sind gerade auf der Suche nach Fördergeldern und Kooperationspartnern, um den Test zur Validierung zu bringen. Mit eigenen Mitteln kann der Verein dies leider nicht. Aber die Aussichten auf eine Förderung sind gut und wir sind sehr zuversichtlich, die Validierung in den nächsten fünf Jahren zu bekommen.
InVitroJobs: Wie ist die Reaktion der Industrie auf den Test?
Prof. Schrage: Die Industrie ist sehr interessiert an unserem Test und es gab auch bereits Förderungen durch die Colipa (Verband der europäischen Kosmetikhersteller) und die EPAA (Europäischer Verband der Waschmittelhersteller). Die Industrie möchten wir auf jeden Fall auf dem Weg zur Validierung des Verfahrens mit einbinden. Ganz besonders ist die Pharmaindustrie an der Testung interessiert, da sich hier eine einfache Methode herauskristallisiert hat, im Vorfeld valide Daten über Wirkungen und Nebenwirkungen der Galenik zu erheben sowie die Pharmakokinetik der isolierten Hornhaut im Einfach-, Wiederholungs- und Sättigungsversuch an einer einzigen Hornhaut durchführen zu können.
InVitroJobs: Bilden Sie Studenten in der Entwicklung bzw. Anwendung des Tests bzw. in Ersatzverfahren zum Tierversuch aus?
Prof. Schrage: Nein, zurzeit nicht. In der Vergangenheit haben insgesamt acht Doktoranden diesen Test gelernt und selbstständig bearbeitet.
InVitroJobs: Wir danken für das Gespräch.
Glossar:
1 Bovine Corneal Opacity/Permeability Assay: Im Test werden Hornhäute von geschlachteten Rindern in eine Apparatur eingespannt. Es erfolgt eine quantitative Messung der Hornhauttrübung (Opacity) und der Durchlässigkeit der Hornhaut mit einem sogenannten Opatcitometer sowie mit einem Spektrophotometer mit sichtbarem Licht (ICCVAM 2006 in EURL ECVAM DB-ALM: Protocol No. 127 (20, 21).
2 Optischer Kohärenztomograf: ähnlich einem Sonografen (Beschreibung siehe Kasten oben).
3 Fluoreszein: ein gelbroter Xanthenfarbstoff, der in alkalischen Lösungen grünlich fluoresziert.
4 Weight-of-evidence-Analyse: Beweiskraftkonzept (22).
5 Isolated Chicken Eye Test (ICE): Test für Substanzen der Kategorie 1. Nutzt Augen von geschlachteten Hühnern. Die Augen werden entkernt und in eine Apparatur eingespannt. Auf die Hornhaut wird die Testsubstanz aufgetragen. Toxische Effekte werden in Form der Trübung der Hornhaut ermittelt, die quantitative Bewertung der Schädigung des Augenepithels durch einen Farbstoffrückhalt (Fluorescein) bestimmt. Zudem wird die Schwellung der Cornea gemessen und makroskopisch eine Beschädigung der Corneaoberfläche untersucht. (23).
6 Human Corneal Epithelium-Test (HCE): Reconstituted Human Corneal Epithelium. Ein dreidimensionales Epithel-Modell aus menschlichen Augenhornhautzellen für den Augenreizungstest (24).
7 HET-CAM Test: Hens egg Test Chorio Allantoic Membrane, Alternativtest zum Draize-Test von 1985. Die Testsubstanz wird auf ein neu Tage bebrütetes Hühnerei gegeben und zwar auf die Chorion-Allantois-Membran. Untersucht wird die Reaktion auf die Substanz in Form von Hämorrhagie, Gefäßlysis und Blutgerinnung (25)
8 Kategorie CAT 1: Gefährdungskategorie des Global Harmonized System (GHS) siehe auch Kasten oben. Kategorie 1: die Substanz kann ernsthafte Augenschädigungen verursachen.
9 Fluoreszenzangiographie: Ein harmloser fluoreszierender Farbstoff wird in das Venensystem am Unterarm injiziert und gelangt in die Netzhaut- und Aderhautgefäße des Auges, wodurch mit einer Spezialkamera Fotoaufnahmen des Augenhintergrundes durchgeführt werden können (26).
10 CAMVA: Chorioallantoic Membrane Vascular Assay, ein Alternativtest am bebrüteten Hühnerei (27)
11 Opazität: Trübung.
12 Endpunkt: in etwa Untersuchungsziel.
13 BfARM: Bundesinstitut für Arzneimittel und Medizinprodukte.
14 SOP: Standard Operation Procedure, eine Art Versuchsdurchführungsvorschrift.
15 ECVAM (EURL ECVAM): Europäisches Referenzlabor des European Center for the Validaton of Alternative Methods (28).
Literatur- und Internetquellen:
(1) http://www.rwth-aachen.de/go/id/bqbt/?#aaaaaaaaaaabqbu
(2) http://idw-online.de/pages/de/news592629
(3) http://www.acto.de/pages/de/projekte/eveit.php#Testprinzip
(4) Spöler, F, Frentz, M, Först, M, Kurz, H & Schrage, NF (2008): Analysis of hydrofluoric acid penetration and decontamination of the eye by means of time-resolved optical coherence tomography. Burns 34: 549-555.
(5) http://www.oecd-ilibrary.org/docserver/download/9712201e.pdf?expires=1405453242&id=id&accname=guest&checksum=8B94846B1CDF0F314ACE10865AA83498
(6) https://web.archive.org/web/20070814145631/http://www.curedisease.com/Perspectives/vol_1_1989/Problems%20with%20the%20Draize.html
(7) http://www.invitrojobs.de/index.php/de/aktuelles-archiv/72-in-vitrobcop-testalsersatzfuertestsankaninchenaugen.html
(8) http://www.invitrojobs.de/index.php/de/aktuelles-archiv/185-arbeitsgruppe-im-portrait-kurzzeit-toxikologie-der-abteilung-experimentelle-toxikologie-und-oekologie-basf.html
(9) http://www.invitrojobs.com/index.php?option=com_content&view=article&id=327:arbeitsgruppe-im-portrait-across-barriers&catid=2:news&Itemid=29
(10) Bock, U., Haltner, E., Guzman, G. & Reichl, S. (2012): Characterisation of Human Cornea Constructs for the Rapid Screening of Preservatives and Evaluation of Their Use in Permeability Assays to Reduce Animal Testing. Abstract zum Kongress für Alternativen zu Tierversuchen, Linz.
(11) Guzman, G., Reichl, S., Bock, U. & Haltner, E. (2012): Optimisation of Human Cornea Constructs For a Rapid Characterisation of Pharmaceutical Preparations, Excipients and Chemical Compounds. Abstract zum Kongress für Alternativen zu Tierversuchen, Linz.
(12) Reichl, S. & Müller-Goymann, C. C. (2004): Künstliche Hornhaut als In-vitro-Modell. http://www.pharmazeutische-zeitung.de/index.php?id=titel_20_2004
(13) Reichl, S., Bednarz, J., C C Müller-Goymann, C. C. (2004): Human corneal equivalent as cell culture model for in vitro drug permeation studies. Br J Ophthalmol. 88: 560–565.
(14) Globally Harmonized System (GHS) of Classification and Labeling of Chemicals Produced by SCHC-OSHA Alliance
GHS Information Sheet Workgroup. Info Sheet #5 Eye Damage / Eye Irritation May, 2010.
(15) http://www.wallstreet-online.de/nachricht/6850030-limbale-stammzellen-hornhaut-nachwachsen
(16) http://www.masseyeandear.org/news/press_releases/recent/2014_Nature_Growing_Corneas/
(17) Ksander, BR, Kolovou, PE, Wilson, BJ, Saab, KR, Guo, Q, Ma, J, McGuire, SP, Gregory, MS, Vincent, WJB, Perez, VL, Cruz-Guilloty, F, Kao, WWY, Call, MK, Tucker, BA, Zhan, Q, Murphy, GF, Lathrop, KL, Alt, C, Mortensen, LJ, Lin, CP, Zieske, JD, Frank, MH, & Frank, NY (2014): ABCB5 is a limbal stem cell gene required for corneal development and repair. Nature Letter. doi:10.1038/nature13426. http://www.nature.com/nature/journal/vaop/ncurrent/full/nature13426.html
(18) http://www.acrossbarriers.de/services/in-vitro-pharmakokinetik/okular/
(19) Adriaens, E, Barroso, J, Eskes, C, Hoffmann, S, McNamee, P, Alépée, N, Bessou‑Touya, S, De Smedt, A, De Wever, B, Pfannenbecker, U, Tailhardat, M & Zuang, V (2014): Retrospective analysis of the Draize test for serious eye damage/eye irritation: importance of understanding the in vivo endpoints under UN GHS/EU CLP for the development and evaluation of in vitro test methods. Arch Toxicol 88: 701–723.
(20) EURL ECVAM DB-ALM: Protocols: Bovine Corneal Opacity and Permeability (BCOP) Assay. DB-ALM Protocol No. 127. http://ecvam-dbalm.jrc.ec.europa.eu/public_view_doc2.cfm?id=9A506ACE702B2EFB9471CBE1CBAA1945579489581FB95A26F52B280413D1D53EA3291B895581F634
(21) http://www.invitrojobs.de/index.php/de/aktuelles-archiv/72-in-vitrobcop-testalsersatzfuertestsankaninchenaugen.html
(22) http://echa.europa.eu/documents/10162/13643/pg_report_weight_of_evidence_de.pdf
(23) http://www.oecd-ilibrary.org/environment/test-no-438-isolated-chicken-eye-test-method-for-identifying-ocular-corrosives-and-severe-irritants_9789264076310-en
(24) Doucet, O, Lanvin, M, Thillou, C, Linossier, C, Pupat, C, Merlin, B & Zastrow, L (2006): Reconstituted human corneal epithelium: A new alternative to the Draize eye test for the assessment of the eye irritation potential of chemicals and cosmetic products. Toxicology in Vitro 20/4: 499–512.
(25) http://pharmazie-lehrbuch.de/kapitel/4-3.pdf
(26) http://www.vincentius-kliniken.de/kliniken-institute/augenklinik/schwerpunkte/fluoreszenzangiographie.html
(27) http://www.mbresearch.com/camva.htm
(28) http://ihcp.jrc.ec.europa.eu/our_labs/eurl-ecvam
Weiterführende Literatur:
(29) Alépée, N, Bessou-Touya, S, Cotovio, J, de Smedt, A, de Wever, B, Faller, C, Jones, P, Le Varlet, B, Marrec-Fairley, M, Pfannenbecker, U, Tailhardat, M, van Goethem, F & McNamee, P. (2013): Cosmetics Europe multi-laboratory pre-validation of the SkinEthic™ reconstituted human corneal epithelium test method for the prediction of eye irritation. Toxicol In Vitro 27(5): 1476-1488.
(30) H. Thomason & D. J. S. Montagnes (2013): Developing a quick and inexpensive in vitro (non-animal) bioassay for mascara irritation. International Journal of Cosmetic Science, 2013, 1–6. doi: 10.1111/ics.12106
(31) Scott L, Eskes C, Hoffmann S, Adriaens E, Alepee N, Bufo M, Clothier R, Facchini D, Faller C, Guest R, Harbell J, Hartung T, Kamp H, Varlet BL, Meloni M, McNamee P, Osborne R, Pape W, Pfannenbecker U, Prinsen M, Seaman C, Spielmann H, Stokes W, Trouba K, Berghe CV, Goethem FV, Vassallo M, Vinardell P, Zuang V (2010) A proposed eye irritation testing strategy to reduce and replace in vivo studies using Bottom-Up and Top-Down approaches. Toxicol In Vitro 24: 1-9
