Leiter der Abteilung Toxikologie(1) ist der Mediziner und Toxikologie Prof. Dr. med. Jan Hengstler. Hier werden die genauen Wirkmechanismen und die gesundheitlichen Auswirkungen von Chemikalien untersucht, denen der Mensch am Arbeitsplatz ausgesetzt sein kann. Die Abteilung ist in vier Arbeitsgruppen unterteilt: Die Systemtoxikologie mit den zwei Nachwuchsgruppen Lebertoxikologie und Zelltoxikologie sowie Neurotoxikologie/ Chemosensorik (2). Die Gruppen Lebertoxikologie, Neurotoxikologie und Zelltoxikologie stellen dabei der Systemtoxikologie ihre Daten für die Weiterentwicklung von Computermodellierungen zur Verfügung. Ein Hauptaugenmerk liegt auf der Entwicklung aussage-kräftigerer und schnellerer Testmethoden.
Foto 1: Mitarbeiter und Mitarbeiterinnen des Forschungsbereichs Toxikologie und Systemtoxikologie.
Fotoquelle: IfADo
Forschung an neuen Methoden zum Ersatz von Tierversuchen
Um Tierversuche zu vermeiden oder zumindest zu reduzieren, forschen die IfADo-Wissenschaftler an der Entwicklung von neuen Methoden zum Ersatz von Tierversuchen. Die Nachwuchsforschergruppe um Dr. Rosemarie Marchan z.B. hat, gemeinsam mit Forschern aus der Schweiz, Belgien und Ägypten hierfür eine Chiptechnologie in der Größe eines Handys entwickelt. Auf die Chipplattform wurden Leber- und Darmorganoide, das sind kleinste Organeinheiten in Kugelform, aufgebracht. Über ein Fließsystem auf dem Chip konnten Medikamente zunächst über die Leberorganoide in die aktive Molekülform verstoffwechselt und anschließend ihre Auswirkungen auf die Darmorganoide untersucht werden (3). Das Forscherteam hat für die Entwicklung vor wenigen Monaten den Global 3R Award erhalten.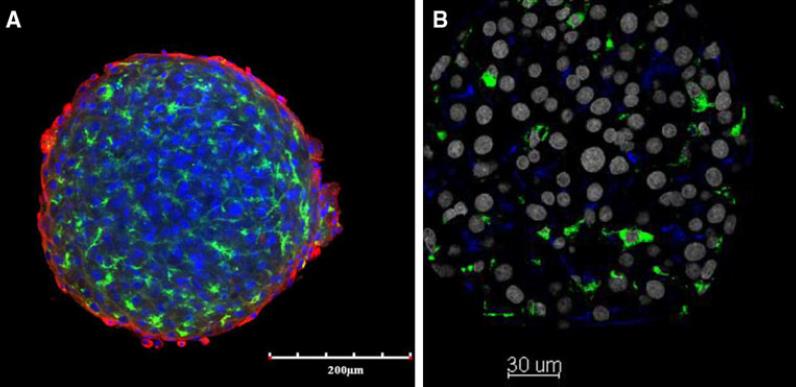
Foto 2: Leber-Organoide. A. Der Organoid aus Hepatozyten enthält einen Überzug aus Endothelzellen und bildet Gallenkanälchen aus (grün). Mit solchen Systemen kann untersucht werden, ob Substanzen in die Galle transportiert werden oder ob sie den Transport von Gallensalzen hemmen. B. In den Organoid wurden zusätzlich noch bestimmte Immunzellen (Kupfferzellen, grün) integriert. Dies ist Teil zurzeit stattfindender Forschungsinitiativen, um Immunfunktionen in Organoide zu integrieren.
Fotoquelle: Hengstler, IfADo
Bei dem Verfahren werden die Organoide in die schräg gestellte Plattform eingeträufelt und fließen in die jeweils vorgesehenen Vertiefungen auf der Plattform. In Mikrovertiefungen wurden die beiden in Reihe angeordneten Gewebetypen hintereinander mit einer Nährflüssigkeit über einen Mikrokanal versorgt und kultiviert. Nach acht Tagen Kultur werden die Organoide der Testflüssigkeit – ein Chemotherapeutikum – ausgesetzt. Das Therapeutikum wirkt zytotoxisch, indem es erst von der Leber vom fremdstoffmetabolisierenden Enzym Cyp2B6 in 4-Hydroxy-Cyclophosphamid transformiert und zum Zielorgan (z.B. einem Lebertumor) weitertransportiert wird. Dort wird es dann in Acrolein umgewandelt (4) und bindet an die DNA (genannt Adduktierung). Infolgedessen wird ein Zelltodmechanismus (Apoptose) in Gang gesetzt. Die (Krebs)Zellen sterben ab (5). Die Wissenschaftler konnten bestätigen, dass dies auch in den kleinen organähnlichen Systemen der Fall ist. Die Fließgeschwindigkeit kann über den Kippwinkel der Chipplattform reguliert werden. Nach Durchfluss der Testsubstanz werden alle Organoide immunhistochemisch gefärbt und z.B. mit einem konfokalen Lasermikroskop untersucht.
Trotz des Erfolges weisen die Wissenschaftler darauf hin, dass es diverse Unterschiede zwischen Leberzellen im natürlichen Organ und Leberzellen gibt, die z.B. aus induzierten pluripotenten Stammzellen gezüchtet worden sind.
Leberzellen derzeit nur ähnlich
Die Vielkönner iPSZ (induzierte pluripotente Stammzellen) können heutzutage relativ leicht zum Beispiel aus Hautzellen von Probanden oder Patienten gewonnen werden. Eine noch nicht immer zufriedenstellend gelöste Herausforderung besteht anschließend in der Umprogrammierung in den gewünschten Zelltyp. Dies ist nicht nur für Fragestellungen zum Ersatz von Tierversuchen notwendig, sondern Forscher versprechen sich auch eine Perspektive zur Behandlung von Lebererkrankungen z.B. durch eine Stammzelltherapie oder eine in ferner Zukunft legende Transplantation eines künstlich geschaffenen Ersatzorgans.
Die über iPSZ gewonnenen Leberzellen ähneln jedoch den natürlichen Zellen lediglich. Für die IfADo-Forscher ist es daher wichtig, Methoden zu entwickeln, um diese Unterschiede bis ins kleinste Detail aufzuspüren und zu ergründen.
In einem Forschungsprojekt mit Kooperationspartnern von der Universität Saarbrücken, der Berliner Charité, der TU Dortmund sowie Experten aus Großbritannien und Schweden führten IfADo-Wissenschaftler sogenannte Gennetzwerk-Analysen mit leberzellähnlichen Zellen durch, entwickelt aus menschlichen embryonalen Stammzellen und induzierten pluripotenten Stammzellen, und verglichen die Ergebnisse mit denen von frisch isolierten humanen Leberzellen (6). Für alle Genexpressionsanalysen wurden dabei zunächst Microarray-Untersuchungen durchgeführt, anhand derer die Forscher sehen können, welche von den rund 22.000 Genen des Menschen in den verschiedenen Zelltypen aktiv sind. Die Ergebnisse wurden mit einem CellNet-Computeralgorithmus analysiert.
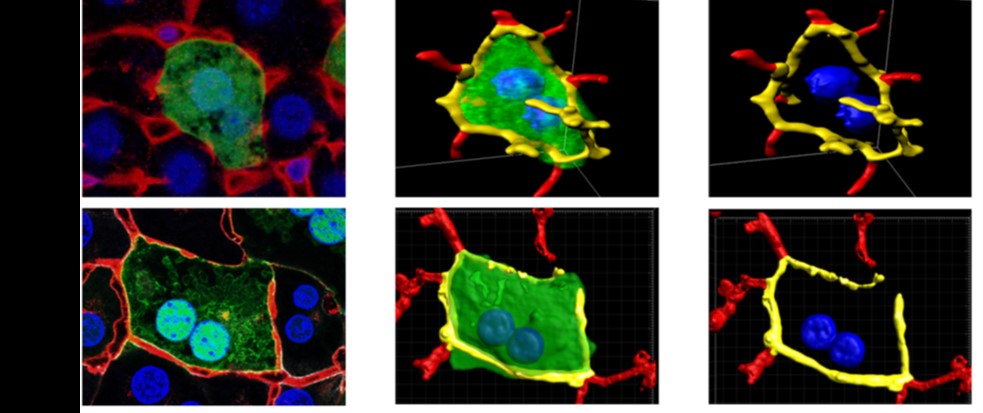
Foto 3: Vergleich von Leberzellen in einer echten Leber (oben) und in kultivierten Hepatozyten (unten). Die linken Abbildungen zeigen die Rohdaten aus dem Mikroskop. In der Mitte sind Rekonstruktionen gezeigt, wobei das Zytoplasma grün, die Zellkerne blau (Hepatozyten haben oft zwei Kerne) und die Gallenkanälchen gelb dargestellt wurden. In den rechten Abbildungen wurde zur besseren Darstellung der Gallenkanälchen das Zytoplasma ausgeblendet. Sowohl in vivo als auch in vitro bilden die Hepatozyten Gallenkanälchen aus und zeigen eine ähnliche Morphologie.
Fotoquelle: Hengstler, IfADo
Sie fanden heraus, dass Leberzell-ähnliche Zellen von ihren Eigenschaften her eine Mischung aus Leber-, Dünndarm-, Bindegewebe- und Stammzellen darstellen, also eine Art Multiorgan-Zelltyp sind. Die erzeugten Zellen gleichen jedoch nur zu 68 Prozent echten Leberzellen. Für toxikologische Untersuchungen werden aber reife Leberzellen mit all ihren Stoffwechseleigenschaften benötigt. Beobachtet wurde, dass die aus Stammzellen abgeleiteten Leberzell-ähnlichen Zellen auch Transkriptionsfaktoren1 bilden, die eine in diesem Fall unerwünschte Entwicklung in Richtung Darm verursachen. Ziel ist es, die Differenzierung von Stammzellen in Leberzellen zu verbessern und verbesserte in-vitro-Testsysteme zu entwickeln, die den Tierversuch in der Toxizitätsprüfung ablösen (7).
Forschung mit praktischem Anwendungsbezug
Die Forschungsergebnisse finden praktische Anwendung z.B. in Kommissionen zur Beurteilung Maximaler Arbeitsplatzkonzentrationen oder in EU-Projekten wie EU-ToxRisk. Hier sollen Machbarkeitsstudien für die Langzeittoxikologie (Lunge, Leber, Niere und Nervensystem) und die Entwicklungs- und Reproduktionstoxikologie mit neuen, humanspezifischen Methoden durchgeführt werden. Zum Einsatz kommen menschliche Zellen, Gewebe oder organähnliche Systeme, omics-Technologien sowie systembiologische Ansätze und Computermodellierungen.
Aufgeklärt werden soll der schädigende Einfluss von Chemikalien auf den Menschen durch mechanistische Untersuchungen von sogenannten Adverse Outcome Pathways (AOPs) in Zellen, Gewebe und Organen. Adverse Outcome Pathways beschreiben einen Vorgang von einem auslösenden molekularen Ereignis, das über einen chemischen Stressfaktor und eine Kaskade biologischer Reaktionen durch verschiedene biologische Ebenen (Organell, Zelle, Gewebe, Organ, Gesamtorganismus) im Laufe der Zeit zu einem schädigenden Effekt führt.
Das EU-Projekt soll am Ende Tierversuche reduzieren, da mit Hilfe tierfreier Methoden toxische Substanzen schon im Vorfeld identifiziert werden können und dadurch nicht erst im Tier bewertet werden (8).
Initiative Virtual Liver
Prof. Hengstler gehört zum wissenschaftlichen Führungsstab innerhalb des Projektclusters Virtual Liver Network, einer nationalen Initiative, die vom BMBF gefördert wird. Ziel dieser Initiative ist es, die Leberphysiologie auf der Ebene einer ganzheitlichen Organbetrachtung darstellen zu können und dadurch zu einem dynamischen Verständnis zu kommen, das nach Möglichkeit in die klinische Praxis übertragen werden kann (9). Im Rahmen dessen hat sich Prof. Hengstler auf die Mechanismen der Leberregeneration konzentriert und hierfür ein Modell entwickelt. Die Initiative Systemmedizin der Leber (LiSyM) ist eine Fortsetzung des Virtual Liver-Projekts mit dem Ziel, den Verlauf einer Lebererkrankung mit Hilfe eines mathematischen Modells vorhersagen zu können.
Aktuell untersucht das Forscherteam um Prof. Hengstler z. B. molekulare Mechanismen, die zu einer Lebererkrankung führen. So laufen ein Projekt zur Rolle des Proteins Rab 18 und dessen Auswirkung auf eine Leberverfettung sowie ein Projekt zur Anpassung eines Computermodells für die Behandlung von chronischen Leberschäden.
"...der ganz große Wurf ist ein sehr komplexes Fernziel..."
Wir befragten Prof. Hengstler zum Stand der gegenwärtigen Entwicklungen im Bereich der humanen Lebermodelle als Ersatz von Tierversuchen in Langzeituntersuchungen und zu seiner Einschätzung im Hinblick auf eine Beendigung der Tierversuche im Bereich der Giftigkeitsprüfungen bis 2025.
InVitro+Jobs:
Zum Ersatz von Tierversuchen in der regulatorischen Toxikologie brauchen Wissenschaftler Zellen, Gewebe oder Organoide, Wie ist hier der Stand der Dinge; welche Tierversuche kann man gut ersetzen und wo gibt es noch Schwierigkeiten?
Prof. Hengstler:
Man kann mit in vitro Methoden schon gut erkennen, ob Substanzen eine erbgutverändernde Wirkung haben, ob sie reizende Effekte auslösen oder ob Enzyme gehemmt oder induziert werden; für diese Untersuchungen hat man in der Vergangenheit Tierversuche benötigt. Schwierig ist es jedoch, Tierversuche zu ersetzen, in denen Substanzen über 28 oder 90 Tage oder länger getestet werden. Das wird zurzeit intensiv erforscht.
InVitro+Jobs:
Wie lange können Wissenschaftler heute Zellen, Gewebe oder organähnliche Systeme kultivieren und in Versuchen nutzen?
Prof. Hengstler:
Es ist relativ einfach, Zellsysteme über ein oder zwei Wochen zu halten. Wenn man Faktoren wie Nährstoffe, Wachstumsfaktoren, pH-Wert und weitere kritische Faktoren konstant hält und eine Kontamination vermeidet, können manche Systeme 3 Monate oder länger kultiviert werden.
InVitro+Jobs:
Bringt diese längere Nutzungsdauer Vorteile? Kann man damit Langzeitversuche ersetzen, bei welchen den Tieren Substanzen über 28, 90 oder gar mehr Tage verabreicht werden?
Prof. Hengstler:
Das ist eine entscheidende Frage, denn alleine dadurch, dass man ein Zellsystem lange in Kultur halten kann, ist ja noch nicht gewährleistet, dass es damit der in vivo Situation, also einem echten Organ im Menschen, ähnlicher wird. Eine weitere, noch nicht beantwortete Frage ist, ob ein Kultursystem, das zum Beispiel über ein Jahr mit einer Leber-schädigenden Substanz behandelt wird, ähnliche Erkrankungen entwickelt, wie die Leber eines Patienten. Nur ein Beispiel: Mache Substanzen führen dazu, dass in der Leber gesunde Leberzellen durch Bindegewebszellen ersetzt werden. Dadurch entstehen Bindegewebsstraßen, welche Blutgefäße einengen. Diese Störung des Blutflusses durch Bindegewebsstraßen kann bis zum Tod führen. Bei den bisher verfügbaren Zell- oder Gewebesystemen werden bei langfristiger Belastung mit Leber-toxischen Substanzen zwar Veränderungen der Zellfunktionen und Zelltod beobachtet, aber die für die Erkrankung der Leberfibrose2 typischen Bindegewebsstraßen konnten bisher nicht nachgestellt werden. Das zeigt, dass diese Gewebesysteme, auch wenn man sie sehr lange in Kultur halten kann, noch nicht genau so reagieren wie ein echtes Organ. Aber etwas anderes ist schon möglich: man kann in einer Kultur mit Leberzellen nach nur einem Tag Exposition gegenüber einer Leber-schädigenden Substanz bereits einen Anstieg bestimmter Biomarker sehen, die man mit einem erhöhten Risiko für Leberfibrose in Zusammenhang bringt. Das verdeutlicht, warum man zur Zeit zwei Strategien verfolgt: die eine sieht den „Nachbau“ von Organen (oder ähnlichen Strukturen) in Kultur vor, um darin dann die Schädigungen und Erkrankungen zu verursachen, wie sie in einem echten Organ auftreten. Die zweite Strategie setzt auf einfachere Zellsysteme und Biomarker; die Ergebnisse werden dann so interpretiert, dass bei Anstieg eines bestimmten Biomarkers im Kurzeitversuch darauf geschlossen wird, dass bei längerer Exposition das Risiko einer Erkrankung erhöht ist. In unserem Labor verfolgen wir beide Strategien und können noch nicht sagen, welche sich schließlich durchsetzen wird, auch wenn wir mit der zweiten Herangehensweise, den einfacheren Systemen zusammen mit gut erforschten Biomarkern, zuletzt bessere Erfolge hatten.
InVitro+Jobs:
Woher nehmen die Wissenschaftler die Kenntnis, dass z.B. ein Miniaturorgan reicht, um das menschliche Organ zu simulieren? Ab wann kann man ein Miniaturorgan oder Zellsystem überhaupt als geeignet ansehen?
Prof. Hengstler:
Um diese Frage zu beantworten haben wir eine Datenbank angelegt, in der wir alle verfügbaren Informationen über Substanzen und ihre Wirkungen auf menschliche Organe gesammelt haben. Zum Beispiel ist bekannt, dass das Medikament Paracetamol fast immer dann zu Leberschäden führt, wenn die Konzentration im Blut einen bestimmten Wert, in diesem Fall ca. 1 Millimolar (mM)3, überschreitet. Wenn also ein in vitro System mit Leberzellen oder eine Miniaturleber bei 1 mM Paracetamol keinen Schaden entwickelt, taugt das System nichts. Zum Glück kann die Giftigkeit von Paracetamol in unseren in vitro Systemen korrekt, d.h. bei der richtigen Konzentration nachgewiesen werden. Wenn man nun dieses Experiment mit einigen hundert Substanzen durchführt, bekommt man einen Überblick über die Genauigkeit und Tauglichkeit des in vitro Systems. Für die überwiegende Mehrheit der Substanzen ist die Vorhersage der in vivo Situation ziemlich genau. Doch bei bestimmten Substanzen würde man bei Einsatz des aktuellen in vitro Systems die Giftigkeit auf die Leber unterschätzen, es versagt in manchen Situationen leider noch.
InVitro+Jobs:
Worin besteht in diesem Fall das Problem?
Prof. Hengstler:
Es besteht darin, dass keines der zurzeit verfügbaren Systeme mit künstlichen Miniorganen über ein richtiges, durchblutetes Kapillarnetzwerk verfügt und dadurch nicht mit Immunzellen interagiert, so wie das im Organismus der Fall ist. Daher versagen zurzeit verfügbare künstliche Minilebern darin, solche giftigen Substanzen zu erkennen, deren Wirkung Immunzellen einbezieht. Eine der nächsten großen Herausforderungen besteht also darin, auch für diese Mechanismen geeignete Vorhersagesysteme zu entwickeln.
InVitro+Jobs:
Ein großes Gebiet in der Forschung zu in vitro Systemen besteht darin, dass man versucht, adulte Körperzellen aus Stamm- oder Vorläuferzellen zu generieren. Was bedeutet es für die Eignung als Ersatz zum Tierversuch, wenn aus Stammzellen entwickelte Hepatozyten-ähnliche Zellen den Leberzellen nur zu 68 Prozent entsprechen?
Prof. Hengstler:
Dieser Ähnlichkeitsscore, hier 68 Prozent, stellt zunächst methodisch einen großen Fortschritt dar. Er wird bestimmt, indem die Boten-RNA (mRNA)4 aller Gene, Menschen haben ca. 22 000 Gene, bestimmt wird. Das geht mit heutigen Analysenmethoden schnell und ist kostengünstig. Dann werden diese mRNAs in Hepatozyten-ähnlichen Zellen, die aus Stammzellen gewonnen worden sind, mit allen mRNAs echter Leberzellen verglichen und daraus nach einer mathematischen Regel einen Ähnlichkeitsscore errechnet. Der Vorteil ist, dass so keine Gene bei der Bewertung ausgelassen werden, der Score stellt somit eine objektive Größe dar. In der Vergangenheit haben nämlich manche Forscher nur solche Gene herausgesucht, für welche eine große Ähnlichkeit zu echten Hepatozyten erreicht wird und haben dadurch ein zu optimistisches Bild erhalten. In der Praxis bedeuten jedoch 68%, dass wir von echten Hepatozyten noch zu weit entfernt sind. Daher setzen wir zurzeit in unseren in vitro Systemen immer noch kultivierte primäre, d.h. ursprünglich aus menschlichen Lebern isolierte Hepatozyten ein. Es wäre ein großer Fortschritt, wenn wir endlich die einfacher verfügbaren Hepatozyten aus Stammzellen verwenden könnten. Doch das macht frühestens dann Sinn, wenn wir einen Ähnlichkeitsscore von mindestens 90% erreicht haben werden.
InVitro+Jobs:
Welche Faktoren müssten gegeben sein, damit sich die Zellen so „wohlfühlen", dass diese Ähnlichkeitsscores in die Höhe gehen?
Prof. Hengstler:
Wir verfolgen dazu zwei Strategien. Einmal wissen wir, welche Kontrollfaktoren, besonders Transkriptionsfaktoren von Genen, in den zurzeit verfügbaren Hepatozyten-ähnlichen Zellen zu wenig bzw. zu sehr aktiv sind. Daher versuchen wir in einem unserer Projekte, diese hyper- bzw. hypoaktiven Transkriptionsfaktoren in den richtigen Zustand zu bringen. Eine zweite Strategie besteht darin, dass wir die Mikroumgebung der echten Leber mit ihrem komplexen Muster an Zytokinen, Chemokinen und ihrer extrazellulären Matrix in vitro nachstellen. Je nachdem wie vielversprechend die Ergebnisse sind, werden wir dann beide Strategien verbinden.
InVitro+Jobs:
Forscher versuchen, die wichtigsten Organe des Menschen im Miniformat nachzuzüchten und miteinander zu verbinden, um einen systemischen Ansatz simulieren zu können. Amerikanische Forscher* berichten davon, bereits 12 Organe miteinander verbinden zu können. Wie ist der gegenwärtige Stand bei der Entwicklung von künstlichen Geweben und Miniorganen zum Ersatz von Tierversuchen in Europa?
Prof. Hengstler:
Nach den Fortschritten auf dem Gebiet der Mikrofluidik haben wir diese Technik genutzt, um mehrere Organsysteme in vitro zu verbinden, z. B. in unseren Arbeiten Frimat et al., 2011 (10) oder Frey et al., 2014 (11). Ein Vorzug dieser fluidischen Systeme ist, dass man die Flüsse steuern kann; so kann das Medium erst durch eine Minileber fließen, bestimmte Chemikalien werden dort metabolisch aktiviert, d.h. erst in den giftigen Zustand überführt, und gelangen dann in ein anderes Organ, in welchem sie toxische Wirkungen entfalten. Auch wesentlich komplexere Flusssysteme sind möglich. Nachdem dies gut funktioniert hat, haben auch amerikanische Gruppen sich für die Technologie begeistert. Im Prinzip ist damit eine technische Voraussetzung gegeben, die Kommunikation zwischen Organen zu untersuchen. Doch die kritische Einschränkung besteht meines Erachtens nicht darin, dass man viele in vitro Systeme miteinander verbindet; wenn man möchte wäre es bereits möglich, hunderte Flusszellen miteinander zu verschalten. Das Problem besteht eher darin, dass die einzelnen künstlichen Organe noch kritische Einschränkungen haben; wenn zum Beispiel keine Mikrogefäße vorhanden sind, kann das künstliche Organ nicht richtig mit Immunzellen interagieren; falls eine Innervation (Anm.: Nervenaussattung) fehlt, bringen infundierte Neurotransmitter keinen Nutzen, etc. Daher wenden wir uns zurzeit in erster Linie der Perfektionierung der in vitro Systeme zu, bevor wir diese auf mikrofluidischen Chips wieder zusammenschalten werden.
InVitro+Jobs:
Wie kann man sich ein Vorhersagemodell vorstellen? Welche Daten werden da eingespeist?
Prof. Hengstler:
Vorhersagemodelle oder Systemsimulationen sind im Zusammenhang mit in vitro Systemen sehr wichtig. Durch die Fortschritte der Computerwissenschaften kann man mit Modellrechnungen die Reaktionen von Geweben nachstellen. Das kann sehr hilfreich sein, wenn sehr viele unterschiedliche Faktoren auf einen Endpunkt einwirken, zum Beispiel auf einen Stoffwechselweg. Auf diese Weise haben wir eine Behandlungsmöglichkeit für eine bestimmte Erkrankung, die Hyperammonämie, identifiziert (Ghallab et al., 2016 (12); Schliess et al., 2014, (13)). Durch reines Nachdenken oder konventionelles Rechnen wäre es sehr schwer gewesen, darauf zu kommen.
Weitere Vorhersagemodelle sind die physiologisch-basierten-pharmakokinetischen Modelle, abgekürzt PBPK. Diese Modelle rechnen zum Beispiel aus, welche Konzentrationen einer Substanz im Blut und in den Organen resultieren, wenn man eine bestimmte Dosis oral (über den Mund) aufnimmt. Das ist wichtig, denn in vitro Systeme haben ja weder eine orale Aufnahme noch eine Niere oder Leber bzw. Darm, über welche die Substanz wieder ausgeschieden wird. Daher kann man mit PBPK Modellen ausrechnen, welche Substanzkonzentrationen man sinnvollerweise im in vitro System einsetzt. Leider sind PBPK-Modelle dann noch relativ ungenau, wenn man wenig über eine Substanz weiß.
Ein dritter Modelltyp leitet aus der Ähnlichkeit der chemischen Struktur ab, welche Toxizität vorliegen könnte, zum Beispiel ob eine erhöhte Wahrscheinlichkeit vorliegt, dass das Erbgut verändert wird. Die Genauigkeit dieser Vorhersagesysteme hängt besonders davon ab, wie gut und umfassend die Datenbasis ist, von der sie abgeleitet wurden.
Bei allen Einschränkungen, welche diese Vorhersagemodelle noch haben, halte ich sie trotzdem für sehr wichtig. Wahrscheinlich werden größere Fortschritte in Zukunft durch eine kluge Verbindung von in vitro Systemen mit geeigneten Modellsimulationen gelingen.
InVitro+Jobs:
Falls die Daten von Prädiktionsmodellen auf Tierversuchsergebnissen basieren: gibt es da nicht wieder Probleme hinsichtlich der Vergleichbarkeit durch Speziesunterschiede?
Prof. Hengstler:
Das sehe ich auch so: Tierversuche (oder auch Strategien mit in vitro Systemen, die auf Tierzellen basieren), haben das Problem der Interspeziesunterschiede zu berücksichtigen. Hierfür gibt es bereits gute aber nicht perfekte Techniken der Interspeziesextrapolation5. In vitro Systeme generell, auch auf menschlichen Zellen basierende, müssen sich mit der Schwierigkeit auseinandersetzen, wie man vom einfacheren in vitro System auf die komplexere in vivo Situation extrapoliert. Zurzeit erreicht man immer noch das größte Maß an Sicherheit für Menschen, wenn man die Vorzüge beider Strategien verbindet.
InVitro+Jobs:
Wie schätzen Sie die Perspektive bis zum Jahr 2025 ein? Halten Sie den Ersatz von Tierversuchen auf dem Gebiet der regulatorischen Toxikologie für möglich?
Prof. Hengstler:
Ich gehe davon aus, dass bis 2025 erhebliche Fortschritte möglich sein werden. Einige Informationen über Toxizität, die zurzeit üblicherweise durch Tierversuche ermittelt werden, wird man mit in vitro Tests gewinnen können. Zum Beispiel zeichnet es sich ab, dass es in wenigen Jahren zuverlässige Prä-Tests geben wird. Damit wird man aus vielen Substanzen diejenigen identifizieren können, welche so gefährlich sind, dass man sie am besten gleich aussortiert und gar nicht erst im Tierversuch testen muss. Aber der ganz große Wurf, die vollständige Nachstellung von Menschen und Versuchstieren in vitro und in silico, so dass man überhaupt keine Organismen mehr für Experimente benötigt, ist ein sehr komplexes Fernziel, dessen Lösung zurzeit nicht absehbar ist. Ich könnte mir vorstellen, dass dies eine Herausforderung für Generationen an Wissenschaftlern darstellt.
* Prof. Anthony Atala vom Institut für Regenerative Medizin an der Wake Forest School of Medicine in North Carolina
Literatur/Quellen:
(1) http://www.ifado.de/
(2) http://www.ifado.de/toxikologie/
(3) Jin-Young Kim, David A. Fluri, Rosemarie Marchan, Kurt Boonen, Soumyaranjan Mohanty, Prateek Singh, Seddik Hammad, Bart Landuyt, Jan G. Hengstler, Jens M. Kelm, Andreas Hierlemann & Olivier Frey (2015): 3D spherical microtissues and microfluidic technology for multi-tissue experiments and analysis. Journal of Biotechnology 205: 24–35.
(4) Aktories, K., Förstermann, U., Hofmann, F.B. & Starke, K. (2009): Allgemeine und spezielle Pharmakologie und Toxikologie. Repetitorium. Verlag Urban & Fischer.
(5) Marquardt, H., Schäfer, S. & Barth, H. (2013): Toxikologie. Wissenschaftliche Verlagsgesellschaft, Stuttgart.
(6) Patricio Godoy, Wolfgang Schmidt-Heck, Karthick Natarajan, Baltasar Lucendo-Villarin, Dagmara Szkolnicka, Annika Asplund, Petter Björquist, Agata Widera, Regina Stöber, Gisela Campos, Seddik Hammad, Agapios Sachinidis, Umesh Chaudhari, Georg Damm, Thomas S. Weiss, Andreas Nüssler, Jane Synnergren, Karolina Edlund, Barbara Küppers-Munther, David C. Hay & Jan G. Hengstler (2015): Gene networks and transcription factor motifs defining the differentiation of stem cells into hepatocyte-like cells. Journal of Hepatology 63: 934–942.
(7) http://www.ifado.de/blog/2017/01/04/forschungsprojekt-von-der-stammzelle-zur-leberzelle
(8) http://www.ifado.de/toxikologie/2016/10/10/eu-projekt-gefahrenstoffe-effizienter-und-tierversuchsfrei-bestimmen/
(9) http://network.virtual-liver.de/de/
(10) Frimat, J.P., Becker, M., Chiang, Y.Y., Marggraf, U., Janasek, D., Hengstler, J. G., Franzke, J. & West, J. (2011): A microfluidic array with cellular valving for single cell co-culture. Lab Chip. 11(2): 231-237.
(11) Frey, O., Misun, P.M., Fluri, D.A., Hengstler, J.G. & Hierlemann, A. (2014): Reconfigurable microfluidic hanging drop network for multi-tissue interaction and analysis. Nat Commun. 5: 4250.
(12) Ghallab, A., Cellière, G., Henkel, S.G., Driesch, D., Hoehme, S., Hofmann, U., Zellmer, S., Godoy, P., Sachinidis, A., Blaszkewicz, M., Reif, R., Marchan, R., Kuepfer, L., Häussinger, D., Drasdo, D., Gebhardt, R. & Hengstler, J. G. (2016): Model-guided identification of a therapeutic strategy to reduce hyperammonemia in liver diseases. J Hepatol. 64/4: 860-871.
(13) Schliess, F., Hoehme, S., Henkel, S.G., Ghallab, A., Driesch, D., Böttger, J., Guthke, R., Pfaff, M., Hengstler, J.G., Gebhardt, R., Häussinger, D., Drasdo, D. % Zellmer, S. (2014): Integrated metabolic spatial-temporal model for the prediction of ammonia detoxification during liver damage and regeneration. Hepatology 60/6: 2040-2051.
Glossar:
1 Transkriptionsfaktoren: Ein Protein, das als eine Art "Lesezeichen" an die DNA oder einen Proteinkomplex bindet, wodurch die RNA-Polymerase aktiviert wird und an einer bestimmten Stelle der DNA eine Matritze (Boten-RNA) herstellt.
2 Leberfibrose: Umbauvorgang in der Leber, bei dem Lebergewebe durch Bindegewebe ersetzt wird.
3 Millimolar: Angabe für die Stoffmengenkonzentration, 1 Molar entspricht 1 mol/Liter, d.h. ca. 6.022 mal 10 hoch 23 Teilchen, 1 milliomol 1/1000 Mol.
4 Boten-RNA: ist das Einzelsträngige Transkript eines Teilabschnitts der DNA. Es dient als Matritze für die Herstellung von Proteinen.
5 Interspeziesextrapolation: ein bestimmtes mathematisches Verfahren („Hochrechnung“), nach welchem Testergebnisse von einer anderen Art (Tierspezies) auf den Menschen übertragen werden.




 Dr. rer. nat.
Dr. rer. nat. Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.
Menschen für Tierrechte - Tierversuchsgegner Rheinland-Pfalz e.V.